题目内容
汽车的启动电源常用铅蓄电池,电池反应如下:PbO2+Pb+2H2SO4
2PbSO4+2H2O,根据此反应判断下列叙述中正确的是( )
| 放电 |
| 充电 |
| A、电池放电时,PbO2是负极;充电时,PbO2是电池的阳极 |
| B、负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C、放电时,PbO2得电子,被氧化 |
| D、电池放电时,溶液酸性增强 |
考点:原电池和电解池的工作原理
专题:
分析:该装置放电时,Pb是负极、PbO2是正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,负极反应式为Pb+SO42--2e-=PbSO4,正极反应式为PbO2+2e-+SO42-+4H+=PbSO4+2H2O,充电时是电解池,阴极、阳极反应式与负极、正极反应式正好相反,据此分析解答.
解答:
解:A.电池放电时,Pb是负极、PbO2是正极;充电时,PbO2是电池的阳极,故A错误;
B.负极上Pb失电子发生氧化反应,负极的电极反应式为:Pb+SO42--2e-=PbSO4,故B正确;
C.放电时,PbO2得电子,被还原,发生还原反应,故C错误;
D.根据PbO2+Pb+2H2SO4
2PbSO4+2H2O知,放电时,氢离子参加反应导致溶液中氢离子浓度减小,溶液的pH升高,故D错误;
故选B.
B.负极上Pb失电子发生氧化反应,负极的电极反应式为:Pb+SO42--2e-=PbSO4,故B正确;
C.放电时,PbO2得电子,被还原,发生还原反应,故C错误;
D.根据PbO2+Pb+2H2SO4
| 放电 |
| 充电 |
故选B.
点评:本题考查原电池和电解池原理,会根据充放电确定各个电极上发生的反应是解本题关键,知道正负极、阴阳极反应式的关系,难点是电极反应式的书写.

练习册系列答案
相关题目
向一定量Fe、FeO、Fe2O3的混合物中加入1 000mL 0.1mol?L-1的盐酸,恰好完全溶解,所得溶液中加KSCN无红色出现,若用足量CO还原相同质量的此混合物,能得到铁( )
| A、11.2 g |
| B、2.8 g |
| C、5.6 g |
| D、无法计算 |
下列有机物中,属于高分子化合物的是( )
| A、油 | B、蔗糖 | C、葡萄糖 | D、蛋白质 |
在反应3Cl2+6KOH(浓)
KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为( )
| ||
| A、1:5 | B、4:1 |
| C、5:1 | D、1:4 |
下列物质不会造成大气污染的是( )
| A、二氧化硫 | B、氮气 |
| C、一氧化碳 | D、氮氧化物 |
短周期元素X、Y,其简单离子的电子层结构相同,下列说法中正确的是( )
| A、如果mXa+和nYb-的核外电子数相等,则a+b=n-m |
| B、如果X、Y的简单离子为X2-和Y2+,那么X的最外层电子数一定大于Y |
| C、X和Y一定不是同周期元素 |
| D、若X的原子半径大于Y,则最高正化合价X大于Y |
下列反应中必须加入还原剂才能进行的是( )
| A、O2→OH- |
| B、Zn→Zn2+ |
| C、H2→H2O |
| D、CuO→CuCl2 |
关于 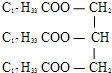 ,下列说法正确的是( )
,下列说法正确的是( )
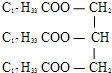 ,下列说法正确的是( )
,下列说法正确的是( )| A、属于油脂,名为硬脂酸甘油酯 |
| B、常温下呈固态 |
| C、属于高分子化合物 |
| D、碱性条件下能发生皂化反应 |