题目内容
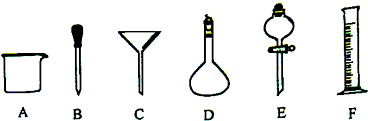
 有A、B、C、D、E、F六种短周期元素,其元素特征信息如表:
有A、B、C、D、E、F六种短周期元素,其元素特征信息如表:| 元素编号 | 元素特征信息 |
| A | A的单质是密度最小的物质 |
| B | B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D与B同周期,该周期中D的简单离子半径最小 |
| E | B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分 |
| F | F元素最高正价与最低负价的代数和为4 |
(2)D、E、F的简单离子半径由大到小的顺序是(用化学式表示)
(3)写出两种均含A、B、C、F四种元素的化合物在溶液中相互反应的离子方程式
(4)一定量的石灰乳中通人一定量的E单质.两者恰好完全反应,生成物中有三种含E元素的离子.其中两种离子的物质的量(n)与反应时间(t)的曲线如下图所示.则t2时刻消耗氢氧化钙质量为
(5)A、B形成的化合物BA在有机合成中用途很广泛.它可以夺取很多化合物中的质子而生成相应的钠化合物.写出它与乙醇反应的化学方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:这几种元素都是短周期元素,A的单质是密度最小的物质,则A是H元素;
B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子,则B是Na元素;
C的原子最外层电子数是其内层电子数的三倍,原子最外层电子不能超过8个,则C最外层电子数是6,其内层电子数是2,为O元素;
D与B同周期,该周期中D的简单离子半径最小,则D是Al元素;
B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分,E原子核外有17个电子,为Cl元素,则Y是NaClO;
F元素最高正价与最低负价的代数和为4,其最高价正化合价与最低负化合价的绝对值之和为8,则F为S元素,
再结合题目分析解答.
B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子,则B是Na元素;
C的原子最外层电子数是其内层电子数的三倍,原子最外层电子不能超过8个,则C最外层电子数是6,其内层电子数是2,为O元素;
D与B同周期,该周期中D的简单离子半径最小,则D是Al元素;
B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分,E原子核外有17个电子,为Cl元素,则Y是NaClO;
F元素最高正价与最低负价的代数和为4,其最高价正化合价与最低负化合价的绝对值之和为8,则F为S元素,
再结合题目分析解答.
解答:
解:这几种元素都是短周期元素,A的单质是密度最小的物质,则A是H元素;
B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子,则B是Na元素;
C的原子最外层电子数是其内层电子数的三倍,原子最外层电子不能超过8个,则C最外层电子数是6,其内层电子数是2,为O元素;
D与B同周期,该周期中D的简单离子半径最小,则D是Al元素;
B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分,E原子核外有17个电子,为Cl元素,则Y是NaClO;
F元素最高正价与最低负价的代数和为4,其最高价正化合价与最低负化合价的绝对值之和为8,则F为S元素,
(1)B是Na元素,Na原子核外有3个电子层、最外层电子数是1,所以Na位于第三周期第IA族,化合物Y为NaClO,NaClO中钠离子和次氯酸根离子之间存在离子键、Cl原子和O原子之间存在共价键,
故答案为:第三周期ⅠA族;离子键和共价键(极性共价键);
(2)D是Al元素、E是Cl元素、F是S元素,电子层数越多其离子半径越大,电子层结构相同的离子,其离子半径随着原子序数增大而减小,所以离子半径大小顺序是S2->Cl->Al3+,
故答案为:S2->Cl->Al3+;
(3)两种均含A、B、C、F四种元素的化合物在溶液中相互反应的物质为亚硫酸氢钠、硫酸氢钠,二者反应离子方程式为H++HSO3-=SO2↑+H2O,故答案为:H++HSO3-=SO2↑+H2O;
(4)根据图象知,溶液中存在的溶质是CaCl2、Ca(ClO)2、Ca(ClO3)2,溶液中ClO-、ClO3-的物质的量分别是0.2mol、0.1mol,根据转移电子守恒得n(Cl-)=n(ClO-)+5n(ClO-)=0.7mol,根据化学式知,n(Ca)=
n(Cl)=
×(0.2mol+0.1mol+0.7mol)=0.5mol,根据Ca原子守恒得n(Ca)=n[Ca(OH)2]=0.5mol,m[Ca(OH)2]=0.5mol×74g/mol=37g,其反应方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O,
故答案为:37;10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O;
(5)A、B形成的化合物BA为NaH,NaH和乙醇反应生成乙醇钠和氢气,反应方程式为NaH+CH3CH2OH=CH3CH2ONa+H2↑,故答案为:NaH+CH3CH2OH=CH3CH2ONa+H2↑.
B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子,则B是Na元素;
C的原子最外层电子数是其内层电子数的三倍,原子最外层电子不能超过8个,则C最外层电子数是6,其内层电子数是2,为O元素;
D与B同周期,该周期中D的简单离子半径最小,则D是Al元素;
B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分,E原子核外有17个电子,为Cl元素,则Y是NaClO;
F元素最高正价与最低负价的代数和为4,其最高价正化合价与最低负化合价的绝对值之和为8,则F为S元素,
(1)B是Na元素,Na原子核外有3个电子层、最外层电子数是1,所以Na位于第三周期第IA族,化合物Y为NaClO,NaClO中钠离子和次氯酸根离子之间存在离子键、Cl原子和O原子之间存在共价键,
故答案为:第三周期ⅠA族;离子键和共价键(极性共价键);
(2)D是Al元素、E是Cl元素、F是S元素,电子层数越多其离子半径越大,电子层结构相同的离子,其离子半径随着原子序数增大而减小,所以离子半径大小顺序是S2->Cl->Al3+,
故答案为:S2->Cl->Al3+;
(3)两种均含A、B、C、F四种元素的化合物在溶液中相互反应的物质为亚硫酸氢钠、硫酸氢钠,二者反应离子方程式为H++HSO3-=SO2↑+H2O,故答案为:H++HSO3-=SO2↑+H2O;
(4)根据图象知,溶液中存在的溶质是CaCl2、Ca(ClO)2、Ca(ClO3)2,溶液中ClO-、ClO3-的物质的量分别是0.2mol、0.1mol,根据转移电子守恒得n(Cl-)=n(ClO-)+5n(ClO-)=0.7mol,根据化学式知,n(Ca)=
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:37;10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O;
(5)A、B形成的化合物BA为NaH,NaH和乙醇反应生成乙醇钠和氢气,反应方程式为NaH+CH3CH2OH=CH3CH2ONa+H2↑,故答案为:NaH+CH3CH2OH=CH3CH2ONa+H2↑.
点评:本题考查位置结构性质的相互关系及应用,涉及氧化还原反应的计算、离子方程式的书写、元素周期律等知识点,综合性较强,难点是(4)题的有关计算,利用原子守恒及转移电子守恒解答,题目难度中等.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
下列混合物中,能够用过滤的方法分离的是( )
| A、铜粉和铁粉 | B、汽油和水 |
| C、泥沙和食盐 | D、食盐和蔗糖 |
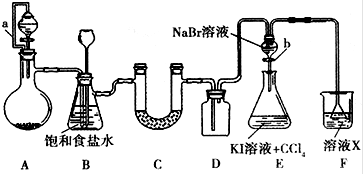
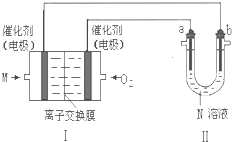 A、B、C、D、E为短周期元素,且原子序数依次递增.其中B元素形成化合物种类最多,A、E同主族.A与 E的质子数之和是B质子数的2倍,且E与D分别形成的最简单离子都含有10个电子.由以上元素组成的物质BD和C2具有相同的电子数.
A、B、C、D、E为短周期元素,且原子序数依次递增.其中B元素形成化合物种类最多,A、E同主族.A与 E的质子数之和是B质子数的2倍,且E与D分别形成的最简单离子都含有10个电子.由以上元素组成的物质BD和C2具有相同的电子数.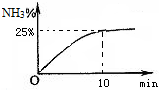 含氮化合物对人类生活有十分重大的意义.
含氮化合物对人类生活有十分重大的意义.