题目内容
5.从经济效益和环境保护的角度考虑,大量制取硝酸铜最宜采用的方法是( )| A. | Cu+HNO3(浓)→Cu(NO3)2 | |
| B. | Cu+HNO3(稀)→Cu(NO3)2 | |
| C. | Cu $\frac{空气}{加热}$ CuO $\frac{硝酸}{\;}$ Cu(NO3)2 | |
| D. | Cu $\frac{浓硫酸}{加热}$ CuSO4 $\frac{硝酸钡}{\;}$ Cu(NO3)2 |
分析 制备硝酸铜不能生成有毒气体,且消耗原料少,操作简单,结合NO、NO2、SO2有毒来解答.
解答 解:A.反应生成有毒气体NO2,故A不选;
B.反应生成有毒气体NO,故B不选;
C.Cu与氧气反应生成CuO,CuO与硝酸反应生成硝酸铜和水,无有毒气体生成,且操作简单,消耗原料少,故C选;
D.Cu与浓硫酸反应生成有毒气体SO2,且消耗浓硫酸、硝酸钡,故D不选;
故选C.
点评 本题考查制备实验方案的评价,为高频考点,把握物质的性质、发生的反应、制备原理为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
15.在一定条件下的定容密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g),下列哪种情况,能表明反应达到平衡状态( )
| A. | SO3的体积百分含量保持不变 | |
| B. | SO2速率是O2速率的2倍 | |
| C. | SO3的浓度是O2浓度的2倍 | |
| D. | 单位时间内SO2消耗的浓度等于SO3生成的浓度 |
16.H2O、BF3 的杂化类型分别是( )
| A. | sp3、sp2 | B. | sp3、sp | C. | sp2、sp | D. | sp2、sp3 |
13.下列描述中正确的是( )
| A. | ClO3-的空间构型为平面三角形 | |
| B. | 乙炔分子中的两个碳原子采用sp2杂化方式 | |
| C. | CS2为V形的极性分子 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |
20.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 60gSiO2中含Si-O键的个数为2NA | |
| C. | 12 g石墨中含有C-C键的个数为1.5NA | |
| D. | 36 g戊烷中共价键的个数为10NA |
10.短周期元素X和Y,可组成化合物XY3.当X的原子序数为a时,Y的原子序数可能是:①a+2,②a+4,③a+8,④a+12,⑤a-6,其中正确的组合是( )
| A. | ①② | B. | ①②③ | C. | ①②③⑤ | D. | ①②④⑤ |
17.用括号中的试剂除去各组中的杂质,正确的是( )
| A. | 苯中的甲苯(溴水) | B. | 溴苯中的溴(苯) | ||
| C. | 乙烷中的乙烯(酸性高锰酸钾) | D. | 95.6%乙醇中的水(生石灰) |
14.下列实验操作能达到预期实验目的是( )
| 实验目的 | 实验操作 | |
| A | 检验FeCl3溶液的Fe2+ | 向溶液中加入酸性KMnO4溶液 |
| B | 比较CH3COOH和HCN的酸性强弱 | 用pH计分别测定CH3COONa、NaCN饱和溶液的pH |
| C | 制备H2SiO3胶体 | 向Na2SiO3溶液中滴加过量HCl |
| D | 除去乙酸乙酯中的CH3COOH | 加入饱和Na2CO3溶液,振荡后静置,分液 |
| A. | A | B. | B | C. | C | D. | D |
20.某化学研究小组利用如图装置探究FeSO4分解后的产物.
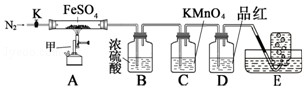
查阅资料得知:SO3溶于水会形成大量的酸雾,工业上通常用浓硫酸做为SO3吸收剂.
实验步骤:按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取m g FeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K.加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的气体,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃.待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末.请回答下列问题:
(1)B中浓硫酸的作用是吸收分解产生的SO3;
(2)实验前通入一段时间N2,目的是排尽装置中的空气;FeSO4完全分解后,还需要通入一段时间N2,原因是将装置内残留的气体排入吸收装置,使其完全被吸收;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化.写出C中发生反应的离子方程式5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
(4)若C中原先加入了20mL 1.00mol/L的KMnO4溶液,为了确定FeSO4分解的化学方程式,某同学进行了如下实验:
I、称量B装置在实验前后增重0.80g;
II、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
III、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点;
IV、重复实验3次,记录数据如表
①滴定至终点的现象溶液由紫红色变为无色且半分钟不恢复成紫红色;
②FeSO4分解的化学方程式为8FeSO4$\frac{\underline{\;高温\;}}{\;}$4Fe2O3+2SO3↑+6SO2↑+O2↑;
(5)请设计一个实验来检验A中的FeSO4是否完全分解将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全.

查阅资料得知:SO3溶于水会形成大量的酸雾,工业上通常用浓硫酸做为SO3吸收剂.
实验步骤:按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取m g FeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K.加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的气体,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃.待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末.请回答下列问题:
(1)B中浓硫酸的作用是吸收分解产生的SO3;
(2)实验前通入一段时间N2,目的是排尽装置中的空气;FeSO4完全分解后,还需要通入一段时间N2,原因是将装置内残留的气体排入吸收装置,使其完全被吸收;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化.写出C中发生反应的离子方程式5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
| 实验 | 滴定管 开始读数 | 滴定 终点读数 |
| 1 | 0 | 19.98 |
| 2 | 0.10 | 20.12 |
| 3 | 0 | 20.16 |
I、称量B装置在实验前后增重0.80g;
II、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
III、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点;
IV、重复实验3次,记录数据如表
①滴定至终点的现象溶液由紫红色变为无色且半分钟不恢复成紫红色;
②FeSO4分解的化学方程式为8FeSO4$\frac{\underline{\;高温\;}}{\;}$4Fe2O3+2SO3↑+6SO2↑+O2↑;
(5)请设计一个实验来检验A中的FeSO4是否完全分解将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全.