题目内容
NA为阿伏加德罗常数,下列物质所含分子数最少的是( )
| A、含NA个分子的二氧化硫 |
| B、0.5 mol氧气 |
| C、标准状况下5.6 L氢气 |
| D、9 g水 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:先根据物质的量与阿伏伽德罗常数、标况下的气体摩尔体积、摩尔质量将各选项转化成物质的量,根据N=nNA可知,物质的量越大,含有的分子数越多,据此完成本题.
解答:
解:将各选项中的量都转化成物质的量,由N=nNA可知,物质的量越小,含有的分子数越小,
A、含NA个二氧化硫分子的二氧化硫的物质的量为1mol;
B、0.5mol氧气;
C、标况下5.6L氢气的物质的量为0.25mol;
D、9g水的物质的量为0.5mol;
所以物质的量最小的是C,
故选C.
A、含NA个二氧化硫分子的二氧化硫的物质的量为1mol;
B、0.5mol氧气;
C、标况下5.6L氢气的物质的量为0.25mol;
D、9g水的物质的量为0.5mol;
所以物质的量最小的是C,
故选C.
点评:本题考查阿伏加德罗常数的有关计算,题目难度中等,阿伏加德罗常数是高考的“热点”,它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容.要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
美国某技术公司开发出纳米级催化剂,可在较低温度下将甲烷转化成乙烯:2CH4(g)?C2H4(g)+2H2(g)△H,已知在降低温度时该反应平衡向左移动,且有下列两个反应(Q1、Q2均为正值):
反应Ⅰ:C(s)+2H2(g)═CH4(g)△H1=-Q1 反应Ⅱ:C(s)+H2(g)═
C2H4(g)△H2=-Q2
则下列判断正确的是( )
反应Ⅰ:C(s)+2H2(g)═CH4(g)△H1=-Q1 反应Ⅱ:C(s)+H2(g)═
| 1 |
| 2 |
则下列判断正确的是( )
| A、△H<0 |
| B、Q2>Q1 |
| C、△H=2(Q1-Q2) |
| D、△H=Q1-Q2 |
实验室制备氯气的反应为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O中,有关该反应的说法正确的是( )
| ||
| A、HCl是氧化剂 |
| B、Cl元素被还原 |
| C、MnO2在反应中失去电子 |
| D、生成1 mol Cl2时有2 mol电子转移 |
用NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A、常温下,1mol CO2含有的氧原子数为2NA |
| B、0.1mol/L的Al2(SO4)3溶液中含SO42-数为0.3NA |
| C、标况下9g水所含分子数为0.5NA |
| D、常温下,2g氦气所含有原子数为0.5NA |
将30mL0.5mol/LNaCl溶液加水稀释到300mL,稀释后溶液中NaCl的物质量浓度为( )
| A、0.03mol/L |
| B、0.3mol/L |
| C、0.05mol/L |
| D、0.04mol/L |
下列离子方程式书写不正确的是( )
| A、石灰乳跟稀硝酸反应:Ca(OH)2+2H+═Ca2++2H2O |
| B、铜粉投入到硝酸银溶液中:Cu+Ag+═Cu2++Ag |
| C、AlCl3溶液中加入少量的氢氧化钠:Al3++3OH-═Al(OH)3↓ |
| D、钠和冷水反应 2Na+2H2O═2Na++2OH-+H2↑ |
下列各个反应,可以应用于工业生产的是( )
| A、钠在氯气中燃烧,生产食盐 |
| B、二氧化锰和浓盐酸共热,制取氯气 |
| C、氯气与消石灰反应,生产漂白粉 |
| D、氢气和氯气混合见光爆炸制氯化氢,再生产盐酸 |
已知石墨的燃烧热为△H1,金刚石的燃烧热为△H2,下列说法正确的是( )
| A、由于燃烧均为放热反应,所以石墨为重要的能源 |
| B、由于燃烧反应放热,所以△H1和△H2均取正值 |
| C、由于石墨和金刚石同为碳元素组成,所以△H1=△H2 |
| D、由于石墨和金刚石属于不同的单质,所以△H1和△H2不等 |
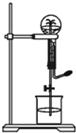 喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?
喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?