题目内容
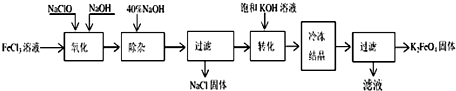
6.金属钛(Ti)的合金具有耐高温、耐腐蚀、强度高等性能,钛合金广泛用于航空、航天工业及化学工业.工业上以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛,同时得到重要的化工原料甲醇(CH3OH).生产的工艺流程图如下(部分产物略去):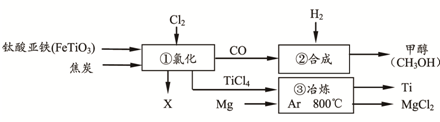
(1)该流程图中涉及到的物质属于有机物的是甲醇(CH3OH).
(2)①中反应为:2FeTiO3+6C+7Cl2一定条件2X+2TiCl4+6CO,则X的化学式为FeCl3.
(3)③所属的基本反应类型为置换.
(4)②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1.
分析 FeTiO3和焦炭在加热条件下通入氯气发生氧化还原反应生成TiCl4、FeCl3和CO,生成的CO和氢气可在一定条件下生成甲醇,TiCl4和Mg在Ar的氛围中加热至800℃可生成Ti和MgCl2,
(1)在物质的组成中含有碳元素的化合物叫有机物,但是一氧化碳、二氧化碳、碳酸钙等具有无机物的性质,属于无机物;
(2)根据质量守恒定律判断;
(3)反应③是四氯化钛和镁在高温的条件下生成氯化镁和钛;
(4)一氧化碳和氢气合成乙醇,反应的方程式为CO+2H2=CH3OH,结合方程式判断.
解答 解:FeTiO3和焦炭在加热条件下通入氯气发生氧化还原反应生成TiCl4、FeCl3和CO,生成的CO和氢气可在一定条件下生成甲醇,TiCl4和Mg在Ar的氛围中加热至800℃可生成Ti和MgCl2,
(1)该流程图中涉及到的物质中属于有机物的只有甲醇,故答案为:甲醇(CH3OH);
(2)根据质量守恒定律可知,在化学反应前后原子个数不变,所以X是FeCl3,故答案为:FeCl3;
(3)反应③是四氯化钛和镁在高温的条件下生成氯化镁和钛,单质和化合物反应生成单质和化合物,属于置换反应,故答案为:置换;
(4)一氧化碳和氢气合成乙醇,方程式为CO+2H2=CH3OH,为使原料全部转化为甲醇,理论上CO和H2投料的质量比为28:4=7:1,故答案为:7:1.
点评 本题以流程图的形式考查物质的制备,为高频考点,需要学生具备综合运用知识及题目信息分析问题、解决问题能力.对于这类题目,需要搞清楚每一步反应物、生成物,清楚工艺流程原理,题目难度中等.

练习册系列答案
相关题目
12.下列各组物质中化学键的类型相同的是( )
| A. | Na2O和Na2O2 | B. | N2和Ne | C. | MgCl2和Na2S | D. | HCl和NaOH |
18.工业制取硫酸是一个连续的生产过程.今测得进入接触室时混合气体(396K、40000kPa,主要成分为SO2、O2、N2)的流量为1.0m3/s,从接触室导出气体(792K、40000kPa)的流量为1.8m3/s,据此,以下说法中正确的是( )
| A. | SO2的催化氧化反应是吸热反应 | |
| B. | SO2的转化率一定为20% | |
| C. | 导出气体中SO3所占的体积分数为$\frac{2}{9}$ | |
| D. | 单位时间内进人接触室的气体与从接触室导出的气体的物质的量之比为10:9 |
15.目前用途最广、用量最大的合金是( )
| A. | 铝合金 | B. | 铁合金 | C. | 铜合金 | D. | 钛合金 |
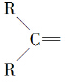 ”生成酮,“
”生成酮,“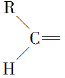 ”生成“
”生成“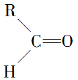 ”,
”,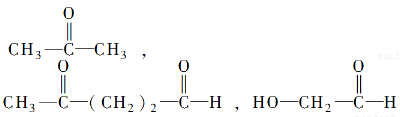
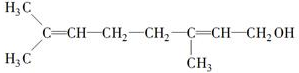 或
或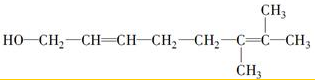 ;
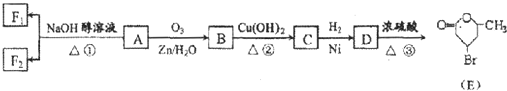
;
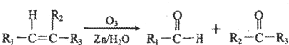
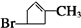
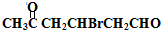 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$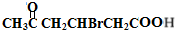 +Cu2O↓+2H2O
+Cu2O↓+2H2O .
.
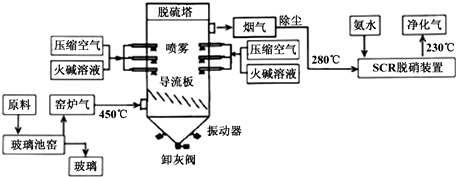
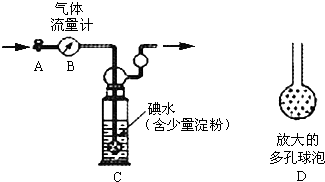 硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放.某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放.某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案: