题目内容
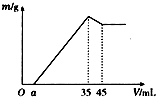 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL某浓度的HCl溶液中(SiO2不溶于HCl溶液),充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量m与加入NaOH溶液的体积的关系如图所示,求:
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL某浓度的HCl溶液中(SiO2不溶于HCl溶液),充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量m与加入NaOH溶液的体积的关系如图所示,求:(1)原溶液中c(HCl)=
(2)若a=2.6mL,计算各组分的质量:m(Al2O3)=
考点:有关混合物反应的计算
专题:计算题
分析:由图象可知,当加入NaOH溶液的体积为35ml时,沉淀的质量达到最大值,则此时溶液的溶质只有NaCl,根据Na元素守恒计算;根据溶解氢氧化铝消耗10ml NaOH溶液,就能知Al(OH)3的物质的量,从而就能求出氧化铝的质量以及二氧化硅的质量.
解答:
解:(1)当加入NaOH溶液的体积为35ml时,n(NaOH)=0.035L×10mol/L=0.35mol,此时沉淀的质量达到最大值,则此时溶液的溶质只有NaCl,根据Na元素守恒,则有:n(HCl)=n(NaCl)=n(NaOH)=0.35mol,
c(HCl)=
=3.5mol/L,故答案为:3.5;
(2)由图象可知,生成的氢氧化铝溶解消耗的NaOH为10ml,设Al(OH)3为 Xmol,
Al(OH)3 ~NaOH
1 mol 1 mol
x mol 10mol?L-1×0.01L
解得x═0.1 mol
而 2Al(OH)3 ~Al2O3 由此可知,n(Al2O3)═0.05 mol,所以m(Al2O3)═5.1g,而铝离子完全沉淀消耗氢氧化钠的物质的量为0.1mol×3=0.3mol,铁离子、铝离子完全沉淀消耗的氢氧化钠溶液的体积为35mL-2.6mL=32.4mL,故该阶段消耗n(NaOH)=0.0324L×10mol/L=0.324mol,故铁离子完全沉淀消耗的氢氧化钠的物质的量为0.324mol-0.3mol=0.024mol,
则铁离子完全沉淀消耗的氢氧化钠的体积为V=
=
=0.0024L=2.4ml,
故n(Fe3+)=
=0.008mol,故m(Fe2O3)=0.008mol×
×160g/mol=0.64g,m(SiO2)=6-0.64-5.1=0.26g;
故答案为:3.50 mol?L-1;5.1;0.26.
c(HCl)=
| 0.35mol |
| 0.1L |
(2)由图象可知,生成的氢氧化铝溶解消耗的NaOH为10ml,设Al(OH)3为 Xmol,
Al(OH)3 ~NaOH
1 mol 1 mol
x mol 10mol?L-1×0.01L
解得x═0.1 mol
而 2Al(OH)3 ~Al2O3 由此可知,n(Al2O3)═0.05 mol,所以m(Al2O3)═5.1g,而铝离子完全沉淀消耗氢氧化钠的物质的量为0.1mol×3=0.3mol,铁离子、铝离子完全沉淀消耗的氢氧化钠溶液的体积为35mL-2.6mL=32.4mL,故该阶段消耗n(NaOH)=0.0324L×10mol/L=0.324mol,故铁离子完全沉淀消耗的氢氧化钠的物质的量为0.324mol-0.3mol=0.024mol,
则铁离子完全沉淀消耗的氢氧化钠的体积为V=
| n |
| c |
| 0.024mol |
| 10mol/L |
故n(Fe3+)=
| 0.024mol |
| 3 |
| 1 |
| 2 |
故答案为:3.50 mol?L-1;5.1;0.26.
点评:本题考查混合物的有关计算,题目难度中等,清楚图象中各阶段发生的反应是关键,注意根据守恒的计算,(3)中注意利用反应判断沉淀最大值时,溶液中的溶质,再利用守恒计算,可以简化计算过程

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
取100mL 0.3mol?L-1和300mL 0.25mol?L-1的硫酸注入500mL容量瓶中,加水稀释至刻度线,该混合溶液中硫酸的物质的量浓度是( )
| A、0.21mol?L-1 |
| B、0.42mol?L-1 |
| C、0.56mol?L-1 |
| D、0.26mol?L-1 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B、常温常压下,由6 g NO2和40 g N2O4组成的混合气体中原子总数为3NA |
| C、0.1 mol?L-1 NaF溶液中,HF和F-总和为0.1NA个 |
| D、12.5 mL 16 mol?L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |
多功能隐形眼镜护理药水的主要成分是双氧水(H2O2),下列有关双氧水的说法正确的是( )
| A、它是由氢气和氧气组成 |
| B、它由两个氢元素和两个氧元素组成 |
| C、每个H2O2分子是由氢元素和氧元素组成 |
| D、每个H2O2分子是由2个氢原子和2个氧原子构成 |
现将ag铁铜镁合金溶于足量的硝酸中,产生的气体是NO、NO2和N2O4的混合物,将该气体与11.2L氧气(标准状况)混合通入足量的水中,气体被完全吸收.向盐酸溶液中加入过量的氢氧化钠溶液,过滤、洗涤、灼烧得到固体的质量为bg.则b-a等于( )
| A、8 | B、16 | C、32 | D、48 |
向Mg(HCO3)2溶液中加入NaOH溶液,可能出现的离子方程式为( )
| A、Mg2++2HCO3-+2OH-→MgCO3↓+CO32-+2H2O |
| B、Mg2++2HCO3-+2OH-→MgCO3↓+2H2O |
| C、Mg2++2HCO3-+4OH-→Mg(OH)2+2CO32-+2H2O |
| D、HCO3-+OH-→CO32-+2H2O |
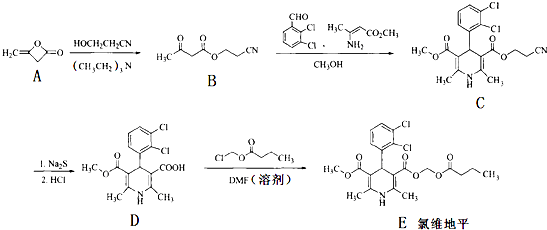
 ]是有机合成中间体,请设计合理的方案以丙酮(
]是有机合成中间体,请设计合理的方案以丙酮(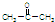 )为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件).
)为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件).