题目内容
将洁净的金属片
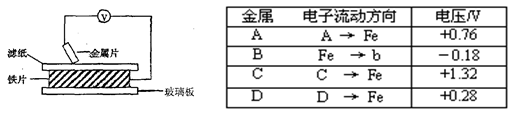
A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).实验时,记录的电压表指针的移动方向和电压表的读数如下表:

已知:构成两电极的金属其金属活泼性相差越大,电压表的读数越大.请依据表中数据判断:
(1)金属________(填代号,下同)可能是最强的还原剂;金属________一定不能从硫酸铜溶液中置换出铜.
(2)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到有蓝色沉淀析出的是金属________.其对应的原电池的电极反应式分别为:负极:________________;正极:________.
答案:
解析:
解析:
|
答案: (1)C B(2)B 2Cu-4e-+4OH- 讲析:(1)首先根据电子的流向判断出,A、C、D比铜活泼,铜比B活泼.再根据电压表的读数可知活泼性顺序为C>A>D>B.(2)欲生成Cu(OH)2沉淀,必须使铜作负极,因此只能是铜与B构成的原电池. |

练习册系列答案
相关题目
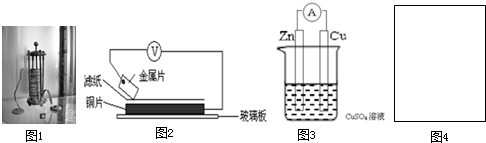
 ”代表反应容器,“
”代表反应容器,“ ”代表导线,“
”代表导线,“ ”代表电极,“
”代表电极,“ ”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.
”代表小灯泡,在右侧方框(图4)内画出装置图并指出电极材料和电解质溶液,标出电源的正负极.
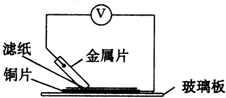 将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录图中电压表指针的移动方向和电压表的读数如下:
将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录图中电压表指针的移动方向和电压表的读数如下: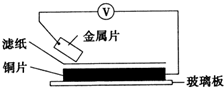 将洁净的金属片A、B、C、D分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下:
将洁净的金属片A、B、C、D分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下: