题目内容
2.水泥是以石灰石和黏土为主要原料制成的硅酸盐产品.含有三种主要成分,下列哪种不在其中( )| A. | .硅酸三钙 | B. | .碳酸二钙 | C. | 铝酸三钙 | D. | .碳酸钙 |
分析 普通水泥的主要原料是粘土、石灰石,在水泥回转窑中反应生成水泥,普通硅酸盐水泥主要成分:3CaO•SiO2、2CaO•SiO2、3CaO•Al2O3,即硅酸三钙、硅酸二钙、铝酸三钙,由此分析解答.
解答 解:普通水泥的主要原料是粘土、石灰石,在水泥回转窑中反应生成水泥,普通硅酸盐水泥主要成分:3CaO•SiO2、2CaO•SiO2、3CaO•Al2O3,即硅酸三钙、硅酸二钙、铝酸三钙,所以ABC都在内,而无碳酸钙,故选D.
点评 本题考查了硅酸盐工业,了解普通硅酸盐水泥的成份,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
5.X、Y、Z、W、M为原子序数依次增大的短周期主族元素.己知:
①元素对应的原子半径大小为:X<Z<Y<M<W;
②Y是组成有机物的必要元素
③Z与X可形成两种常见的共价化合物,与W可形成两种常见的离子化合物;
④M的电子层数与最外层电子数相等.
下列说法不正确的是( )
①元素对应的原子半径大小为:X<Z<Y<M<W;
②Y是组成有机物的必要元素
③Z与X可形成两种常见的共价化合物,与W可形成两种常见的离子化合物;
④M的电子层数与最外层电子数相等.
下列说法不正确的是( )
| A. | W、M的离子半径为M<W | |
| B. | YZ2为直线形的共价化合物,W2Z2既含有离子键又含有共价键 | |
| C. | Z与X形成的化合物的熔沸点偏高是因其分子内存在氢键 | |
| D. | Z与M形成的化合物可作为耐高温材料 |
10.Na2CO3和NaHCO3是金属钠常见的两种碳酸盐,它们广泛地应用于生产和生活中.下列有关碳酸钠和碳酸氢钠的说法中,不正确的是( )
| A. | NaHCO3能中和胃酸,对胃壁不产生强烈的刺激或腐蚀作用,可用于治疗胃酸过多症,但不适合胃溃疡病人 | |
| B. | NaHCO3能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头 | |
| C. | 可以用澄清石灰水来鉴别Na2CO3溶液中和NaHCO3溶液 | |
| D. | 往Na2CO3饱和溶液中通入CO2气体,可获得NaHCO3沉淀 |
17.下列关于一些非金属元素与化合物的说法中,正确的是( )
| A. | 浓硝酸与铜会剧烈反应,浓硝酸起到了氧化剂和酸性的作用 | |
| B. | Cl2溶于水后可以漂白有色布条,且久置后布条可以恢复原色 | |
| C. | 铁遇冷的浓硫酸钝化,说明铁和冷的浓硫酸不会发生反应 | |
| D. | NaOH可与玻璃反应,所以可以用浓NaOH溶液在玻璃上作画 |
14.关于钠及其氧化物性质的叙述中,正确的是( )
| A. | Na能与CuSO4溶液反应置换出红色的铜 | |
| B. | Na2O是碱性氧化物,与酸反应生成盐和水 | |
| C. | Na2O和Na2O2都能与水反应,生成物完全相同 | |
| D. | Na2O2是白色固体,可用于呼吸面具中氧气的来源 |
11.在反应KNO2$\stackrel{△}{→}$K2O+NO↑+O2↑(未配平)中,当生成33.6L NO(标准状况)时,被氧化的氧原子的物质的量为( )
| A. | 3 mol | B. | 1.5 mol | C. | 0.75 mol | D. | 0.6 mol |
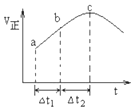 NO2与SO2混合可发生反应:NO2+SO2?SO3+NO.在100℃1molNO2与1molSO2的混合气体置于绝热(不与外界进行热交换)恒容密闭容器中发生上述反应,①正反应速率随时间变化的趋势如图所示,则下列说法正确的是C(填字母).
NO2与SO2混合可发生反应:NO2+SO2?SO3+NO.在100℃1molNO2与1molSO2的混合气体置于绝热(不与外界进行热交换)恒容密闭容器中发生上述反应,①正反应速率随时间变化的趋势如图所示,则下列说法正确的是C(填字母).