题目内容
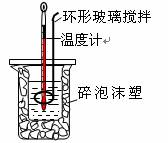
用50 mL0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液,在如图所示的装置中进行中和反应。测定强酸与强碱反应的反应热。

|
|
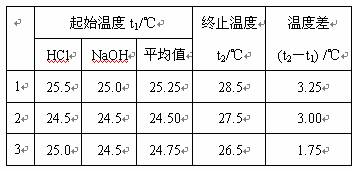
起始温度t1/℃ |
终止温度 t2/℃ |
温度差 (t2-t1) /℃ |
||
|
HCl |
NaOH |
平均值 |
|||
|
1 |
25.5 |
25.0 |
25.25 |
28.5 |
3.25 |
|
2 |
24.5 |
24.5 |
24.50 |
27.5 |
3.00 |
|
3 |
25.0 |
24.5 |
24.75 |
26.5 |
1.75 |
(1)在该实验中,量取50 mL 盐酸或NaOH 溶液,需要用到的玻璃仪器_________。
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是______________________________。
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指______________________________温度。
(4)计算该实验发生中和反应时放出的热量为________________kJ(中和后生成的溶液的比热容c=4.18J/(g·℃ )。
(5) 如果用50 mL 0.55mol/L的氨水(NH3·H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是
________________________ 。
(1)量筒、胶头滴管 (2)减少实验过程中的热量损失
(3)完全反应后混合溶液的最高温度 (4) 1.31 kJ
(5) NH3·H2O是弱电解质,不能完全参加中和反应(或生成的盐会水解,要吸收热量等)
【解析】(1)该实验量取盐酸或氢氧化钠溶液体积的玻璃仪器是量筒和胶头滴管。
(2)该实验过程中应该尽可能的减小热量的损失,所以装置中大、小烧杯之间填满碎泡沫塑料的目的是减少实验过程中的热量损失。
(3)根据实验原理可知,记录的终止温度是指完全反应后混合溶液的最高温度。
(4)根据表中数据可知,实验3的数据误差大,舍去。因此温度变化的平均值是(3.25℃+3.00℃)÷2=3.125℃。溶液的质量是100g,所以反应中放出的热量是4.18J/(g·℃ )×100g×3.125℃=1306.25J=1.31kJ。
(5)△H会偏大,说明反应中放出的热量减少。这是由于NH3·H2O是弱电解质,存在电离平衡,而电离是吸热的。

用50 mL0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液,在如图所示的装置中进行中和反应。测定强酸与强碱反应的反应热。
| | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差 (t2-t1) /℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.5 | 24.50 | 27.5 | 3.00 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是______________________________。
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指______________________________温度。
(4)计算该实验发生中和反应时放出的热量为________________kJ(中和后生成的溶液的比热容c=4.18J/(g·℃ )。
(5) 如果用50 mL 0.55mol/L的氨水(NH3·H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是
________________________ 。
实验室用50 mL0.50 mol/L盐酸、50 mL0.55 mol/LNaOH溶液和下图所示装置
进行测定中和热的实验,得到表中的数据:
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
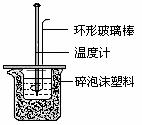
试回答下列问题:
(1)实验时用环形玻璃棒搅拌溶液的方法是_________________________________,
不能用铜丝搅拌棒代替环形玻璃棒的理由是_____________________________。
(2)经数据处理,t2-t1=3.4 ℃。则该实验测得的中和热ΔH = ________________
[盐酸和NaOH溶液的密度按1 g/cm3计算,反应后混合溶液的比热容(c)按4.18
J/(g?℃)计算]。
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为ΔH1,则ΔH1
与ΔH的关系为:ΔH1____________ΔH(填“<”、“>”或“=”),理由是
____________________________________________________。