题目内容
16.下列实验中,所选药品和装置不合理的是( )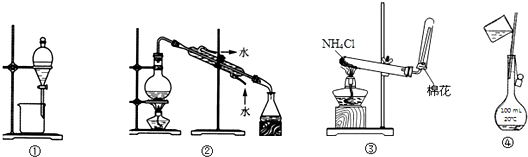
| A. | 选①可用于CC14提取碘水中的碘 | |
| B. | 选②可用于自来水制取蒸馏水 | |
| C. | 选③可用于实验室制取氨气 | |
| D. | 选④可用于配制100 mL 0.1 mol/L NaCl溶液(转移溶液) |
分析 A.如果溶质在不同溶剂中溶解度相差较大,且两种溶剂不互溶,溶质和溶剂不反应,就可以采用萃取的方法分离;
B.可以采用蒸馏的方法制取蒸馏水;
C.加热氯化铵生成氨气与氯化氢,氯化氢与氨气遇冷又生成氯化铵,无法获得氨气;
D.转移液体需要用玻璃棒引流.
解答 解:A.碘在四氯化碳中的溶解度大于在水中的溶解度,且四氯化碳和碘不反应,和水不互溶,所以可用CC14提取碘水中的碘,选①,故A正确;
B.自来水中含有可溶性杂质,且蒸馏时不挥发,水加热易挥发,所以可以采用蒸馏的方法制取蒸馏水,故B正确;
C.氯化铵分解无法获得氨气,实验室用氢氧化钙和氯化铵制取氨气:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3+2H2O,故C错误;
D.转移液体需要用玻璃棒引流,操作合理,故D正确.
故选C.
点评 本题考查实验方案评价,涉及物质的制备和分离和提纯、溶液配制等知识点,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列叙述不正确的是( )D工业上电解饱和食盐水的.
| A. | 铁表面镀锌,锌作阳极 | |
| B. | 船底镶嵌锌块,锌作正极,以防船体被腐蚀 | |
| C. | 钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-═4OH- | |
| D. | 工业上电解饱和食盐水的阳极反应:2Cl--2e-═Cl2↑ |
4.下列反应的离子方程式书写正确的是( )
| A. | 锌粒与醋酸反应:Zn+2H+═Zn2++H2↑ | |
| B. | 铁粉与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| C. | 常温下氯气与烧碱溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
11.下列试剂能用来鉴别乙醇和乙酸的是( )
| A. | 溴水 | B. | 蒸馏水 | C. | 碳酸氢钠溶液 | D. | 氢氧化钠溶液 |
8.下列反应中属于同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应的是( )
| A. | 3Br2+6KOH═5KBr+KBrO3+3H2O | |
| B. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+2H2O+Cl2↑ | |
| C. | 2KNO3 $\frac{\underline{\;\;△\;\;}}{\;}$ 2KNO2+O2↑ | |
| D. | NH4NO3 $\frac{\underline{\;\;△\;\;}}{\;}$ N2O↑+2H2O |
6.常温下,等物质的量浓度,等体积的盐酸分别用pH=9和pH=10的氨水完全中和时,消耗氨水的体积分别为V1和V2,则V1,V2的关系中正确的是( )
| A. | V1=10V2 | B. | V1>10V2 | C. | V1<10V2 | D. | V2>10V1 |

 扁桃酸是重要的医药和染料中间体,其应用非常广泛.扁桃酸的结构简式如图所示.
扁桃酸是重要的医药和染料中间体,其应用非常广泛.扁桃酸的结构简式如图所示.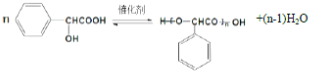 .
.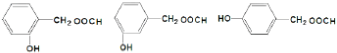 .
.