题目内容
6.向四支试管中分别加入少量不同的无色溶液进行如下操作,则现象及结论都正确的是( )| 操作 | 现象 | 结论 | |
| A | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 滴加氯水和CCl4,振荡、静置 | 上层溶液显橙红色 | 原溶液中有Br- |
| C | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈紫色 | 原溶液中有K+ |
| D | 滴加NaOH溶液,加热,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.硫酸根离子、银离子等滴加BaCl2溶液,都成生成白色沉淀;
B.氯水中的氯气和溴离子反应生成溴单质,四氯化碳把溴从水溶液中萃取出来而显橙红色,四氯化碳的密度大于水,则应该是下层呈橙红色;
C.用洁净铂丝蘸取溶液进行焰色反应,透过蓝色钴玻璃观察,火焰呈紫色说明含有钾离子;
D.滴加稀氢氧化钠溶液,加热,试纸不变蓝,说明原溶液中无铵根离子.
解答 解:A.中滴加氯化钡溶液,有白色沉淀生成,不能说明原溶液中一定含有SO42-,因为SO42-、银离子等滴加氯化钡溶液,都成生成白色沉淀,故A错误;
B.氯水中的氯气和Br-反应生成溴单质,四氯化碳把溴从水溶液中萃取出来四氯化碳密度比水大,下层溶液显橙红色,故B错误;
C.黄色火焰可以覆盖K+的浅紫色火焰,用洁净铂丝蘸取溶液进行焰色反应,透过蓝色钴玻璃观察,火焰呈紫色,证明原溶液中含有钾离子,故C正确;
D.氨气极易溶于水,若不加热,即使溶液中含有少量的NH4+时,滴加稀NaOH溶液也不会放出NH3,故D错误;
故选C.
点评 本题考查了常见离子的性质及检验方法,题目难度中等,明确握常见离子的性质为解答关键,注意检验存在的存在时需要排除其它离子的干扰,确保检验方案的严密性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.在配制一定物质的量浓度的溶液时,不会用到的仪器是( )
| A. | 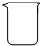 | B. | 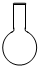 | C. | 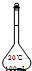 | D. |  |
17.以下实验原理或操作中,正确的是( )
| A. | 将20g硝酸钠和17g氯化钾放入100ml烧杯中,加35mL水,并加热、搅拌,使溶液浓缩至约为原来的一半时,趁热过滤即可得到硝酸钾晶体 | |
| B. | 焰色反应实验中,铂丝在蘸取待测溶液前,应先用稀硫酸洗净并灼烧 | |
| C. | 中和滴定实验中,如用于盛放待测溶液的锥形瓶洗净后未干燥,不影响测定结果 | |
| D. | 移液管取液后,将移液管垂直伸入容器里面,松开食指使溶液全部流出,数秒后,取出移液管 |
18.下列有关氧化还原反应的说法中,正确的是( )
| A. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| B. | 还原剂在反应中发生还原反应 | |
| C. | 氧化还原反应的本质是电子的转移 | |
| D. | 有单质生成的反应一定是氧化还原反应 |
15.雾霾天气对环境造成了严重影响,部分城市开展PM2.5和臭氧(O3)的监测.下列有关说法正确的是( )
| A. | 臭氧的摩尔质量是48 g | |
| B. | 1mol臭氧的体积是22.4L | |
| C. | 16 g臭氧中含有6.02×1023个氧原子 | |
| D. | 已知每个氧原子内有8个质子,那么1 mol臭氧中含有3mol质子 |
5.向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 滴加AgNO3溶液 | 生成白色沉淀 | 原溶液中有Cl- |
| B | 滴加盐酸溶液 | 产生无色无味气体使澄清石灰水变浑浊 | 原溶液中有CO32- |
| C | 滴加硫酸钠和稀硝酸溶液 | 产生白色沉淀 | 原溶液中有Ba2+ |
| D | 滴加稀NaOH溶液 | 生成白色沉淀 | 原溶液中一定有Mg2+ |
| A. | A | B. | B | C. | C | D. | D |