题目内容
下列有关晶体的叙述中,不正确的是( )
| A、干冰晶体中,每个CO2分子周围紧邻10个CO2分子 |
| B、氯化钠晶体中,每个Na+周围距离相等的Na+共有12个 |
| C、氯化铯晶体中,每个Cs+周围紧邻8个Cl- |
| D、金刚石网状结构中,共价键形成的碳原子环中,最小的环上有6个碳原子 |
考点:晶胞的计算
专题:化学键与晶体结构
分析:因为干冰、氯化钠、氯化铯、金刚石的晶胞结构图分别如图所示: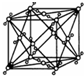 、
、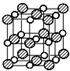 、
、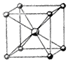 、
、 ;根据干冰、氯化钠、氯化铯、金刚石的晶胞结构可作判断;
;根据干冰、氯化钠、氯化铯、金刚石的晶胞结构可作判断;
 、
、 、
、 、
、 ;根据干冰、氯化钠、氯化铯、金刚石的晶胞结构可作判断;
;根据干冰、氯化钠、氯化铯、金刚石的晶胞结构可作判断;解答:
解:A、干冰的晶胞结构如图所示: ,在立方体的面心上和顶点上都有CO2分子,以上底面心上的CO2分子为例,与之距离最近的同层上的四个CO2分子距离为面对角线的
,在立方体的面心上和顶点上都有CO2分子,以上底面心上的CO2分子为例,与之距离最近的同层上的四个CO2分子距离为面对角线的
,另外在侧面面心上的四个CO2分子与上底面面心上的CO2分子的距离也面对角线的
,另外,在上底面上方的晶胞中四个侧面面上的CO2分子也与上底面面上的CO2分子的距离也面对角线的
,所以每个CO2分子周围最近的CO2分子的个数为12,故A错误;
B、氯化钠晶胞结构如图所示 ,Na+在晶胞中的位置与干冰中二氧化碳分子的位置相似,每个Na+周围距离相等的Na+共有12个,故B正确;
,Na+在晶胞中的位置与干冰中二氧化碳分子的位置相似,每个Na+周围距离相等的Na+共有12个,故B正确;
C、氯化铯晶胞结构如图所示 ,Cs+位于晶胞立方体的体心,在立方体的八个顶点都有一个Cl-,所以每个Cs+周围紧邻8个Cl-,故C正确;
,Cs+位于晶胞立方体的体心,在立方体的八个顶点都有一个Cl-,所以每个Cs+周围紧邻8个Cl-,故C正确;
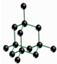
D、金刚石的晶胞结构如图所示: ,所以共价键形成的碳原子环中,最小的环上有6个碳原子,故D正确;
,所以共价键形成的碳原子环中,最小的环上有6个碳原子,故D正确;
故选:A.
 ,在立方体的面心上和顶点上都有CO2分子,以上底面心上的CO2分子为例,与之距离最近的同层上的四个CO2分子距离为面对角线的
,在立方体的面心上和顶点上都有CO2分子,以上底面心上的CO2分子为例,与之距离最近的同层上的四个CO2分子距离为面对角线的| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
B、氯化钠晶胞结构如图所示
 ,Na+在晶胞中的位置与干冰中二氧化碳分子的位置相似,每个Na+周围距离相等的Na+共有12个,故B正确;
,Na+在晶胞中的位置与干冰中二氧化碳分子的位置相似,每个Na+周围距离相等的Na+共有12个,故B正确;C、氯化铯晶胞结构如图所示
 ,Cs+位于晶胞立方体的体心,在立方体的八个顶点都有一个Cl-,所以每个Cs+周围紧邻8个Cl-,故C正确;
,Cs+位于晶胞立方体的体心,在立方体的八个顶点都有一个Cl-,所以每个Cs+周围紧邻8个Cl-,故C正确;D、金刚石的晶胞结构如图所示:
 ,所以共价键形成的碳原子环中,最小的环上有6个碳原子,故D正确;
,所以共价键形成的碳原子环中,最小的环上有6个碳原子,故D正确;故选:A.
点评:本题主要考查各种类型晶体的晶胞的结构,难度较小,解题是要学生能熟记各种典型晶胞的结构.

练习册系列答案
相关题目
下列各组离子中,能在溶液中大量共存的是( )
| A、Na+ H+ NO3- Fe2+ |
| B、Ca2+ NO3- HCO3- OH- |
| C、K+ H+ Cl- SO42- |
| D、Fe3+ Cl- H+ CO32- |
下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
| A、汽车底盘喷涂高分子膜 |
| B、金属护栏表面涂漆 |
| C、水中的钢闸门连接电源的负极 |
| D、地下钢管连接锌块 |
下列变化的比较,不正确的是( )
| A、酸性强弱:HClO4>H2SO4>H3PO4 |
| B、原子半径大小:Na>S>O |
| C、碱性强弱:KOH>NaOH>LiOH |
| D、还原性强弱:F->Cl->I- |
氨溶于水的喷泉实验可以证明( )
| A、氨气比空气轻 |
| B、氨气有刺激性气味 |
| C、氨气不稳定 |
| D、氨气易溶于水 |
下列物质中,既含有离子键又含有共价键的是( )
| A、H2O |
| B、HCl |
| C、NaCl |
| D、NaOH |
对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)△H<0 的化学反应下列叙述不正确的是( )
| A、该反应是放热反应 |
| B、△H的值与反应方程式的计量系数有关 |
| C、若将该反应设计成原电池则锌为负极 |
| D、若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L |
铅蓄电池在放电时起原电池的作用,充电时起电解池的作用.铅蓄电池在放电和充电时发生的化学反应为:Pb+PbO2+2H2SO4
2PbSO4+2H2O,下列叙述正确的是( )
| 放电 |
| 充电 |
| A、放电时的正极反应式:Pb+SO42--2e-═PbSO4 |
| B、放电一段时间后,正极周围溶液的酸性增大 |
| C、充电时的阳极反应式:PbSO4+2H2O-2e-═PbO2+4H++SO42- |
| D、充电时,要使2mol PbSO4变为Pb和PbO2需要通过4mol电子 |