题目内容
20.如图甲是利用一种微生物将废水中的尿素(H2NCONH2)的化学能直接转化为电能,并生成对环境友好物质的装置,同时利用此装置产生的电能对乙装置进行铁上镀铜的实验.下列说法中不正确的是( )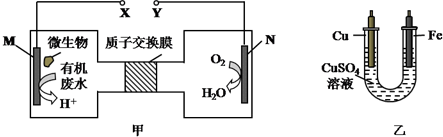
| A. | H+透过质子交换膜由左向右移动 | |
| B. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| C. | 铁电极应与X相连接 | |
| D. | 当N电极消耗0.5mol气体时,则铁电极增重32g |
分析 由题给信息可知,该装置是将化学能转化为电能的原电池,由甲图可知,M是负极,N是正极,电解质溶液为酸性溶液,负极上失电子发生氧化反应,正极上得电子发生还原反应,在铁上镀铜,则铁为阴极应与负极相连,铜为阳极应与正极相连,根据得失电子守恒计算,以此解答该题.
解答 解:该装置是将化学能转化为电能的原电池,由甲图可知,M是负极,N是正极,电解质溶液为酸性溶液,负极上失电子发生氧化反应,正极上得电子发生还原反应,
A.M是负极,N是正极,H+透过离子交换膜由左M极移向右N极,故A正确;
B.H2NCONH2在负极M上失电子发生氧化反应,生成氮气、二氧化碳和水,电极反应式为H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+,故B正确;
C.铁上镀铜,则铁为阴极应与负极相连,故C正确;
D.当N电极消耗0.5 mol氧气时,则转移0.5×4=2mol电子,所以铁电极增重$\frac{2mol}{2}$×64g/mol=64g,故D错误;
故选D.
点评 本题考查了原电池原理以及电镀原理,为高频考点,侧重于学生的分析、计算能力的考查,明确原电池正负极上得失电子、电解质溶液中阴阳离子移动方向即可解答,题目难度中等.

练习册系列答案
相关题目
10.常温时向0.01mol/L 的盐酸溶液中加入等体积的下列溶液,滴入酚酞试液显红色,该溶液是( )
| A. | pH=12的Ba(OH)2溶液 | B. | pH=12的氨水 | ||
| C. | 0.01mol/L AgNO3溶液 | D. | 0.005mol/L NaOH溶液 |
11.2012年7月21日,北京地区突降近60年最大的暴雨,造成水灾.为确保大灾之后无大疫,当地防疫部门使用了含氯类消毒剂,其中ClO2是一种消毒杀菌效率较高的消毒剂,有强氧化性.工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化制得.则有关此反应的说法正确的是( )
| A. | NaClO3是还原剂 | |
| B. | 氧化性:ClO2>NaClO3 | |
| C. | 化学反应方程式为:2NaClO3+Na2SO3+H2SO4=2ClO2+2Na2SO4+H2O | |
| D. | 1 mol NaClO3参加反应有2 mol e-转移 |
15.如图所示,甲池的总反应式O2+N2H4═2H2O+N2.有关该装置工作时,说法正确的是( )
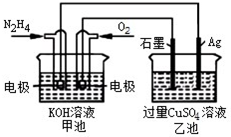

| A. | 甲池中,负极反应为N2H4-4e-═4H++N2 | |
| B. | 甲池溶液pH 保持不变,乙池溶液pH 减小 | |
| C. | 甲池中消耗2.24LO2,此时乙池中理论上多产生12.8g 固体 | |
| D. | 反应一段时间后,向乙池中加一定量CuO 固体,能使CuSO4溶液恢复到原浓度 |
5.下列说法不正确的是( )
| A. | 推广使用氢能、太阳能,减少化石燃料的使用,有助于减少雾霾天气的发生 | |
| B. | 将太阳能转化为氢能是减少污染、缓解能源危机的一种构想 | |
| C. | 石油的分馏、催化裂化、裂解等石油的加工方法,其目的均为得到更多的汽油 | |
| D. | 煤干馏可以得到煤焦油,煤焦油进一步分离又可得到苯、甲苯等有机物 |
18.下列反应属于取代反应的是( )
| A. | 乙烯使溴的四氯化碳溶液褪色 | |
| B. | 苯与液溴在催化剂作用下生成溴苯 | |
| C. | 乙烯与氢气在催化剂作用下生成乙烷 | |
| D. | 乙醇在铜催化、加热条件下与氧气反应 |
19.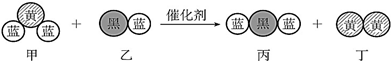 汽车尾气中常常含有CO、NOx等气体,为减轻污染,当代汽车都加装了“三效催化净化器”,可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法不正确的是( )
汽车尾气中常常含有CO、NOx等气体,为减轻污染,当代汽车都加装了“三效催化净化器”,可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法不正确的是( )
 汽车尾气中常常含有CO、NOx等气体,为减轻污染,当代汽车都加装了“三效催化净化器”,可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法不正确的是( )
汽车尾气中常常含有CO、NOx等气体,为减轻污染,当代汽车都加装了“三效催化净化器”,可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法不正确的是( )| A. | 甲、乙、丙、丁中有3 种非极性分子 | |
| B. | 甲和丁中同种元素化合价不相等 | |
| C. | H2CO3、HNO3的相对强弱与分子中键的极性相关 | |
| D. | N2O5的水化物中不存在氢键 |
