题目内容
离子液体是一种室温熔融盐,为非水体系。由有机阳离子、Al2Cl7—和AlCl4—组成的离子液体作电解液时,可在钢制品上电镀铝。
(1)钢制品应接电源的 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为 。若改用AlCl3水溶液作电解液,则阴极产物为 。
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还原产物的物质的量为 mol。
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有 。
a.KCl b. KClO3 c. MnO2 d. Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象, (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是 (用离子方程式说明)。
练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目


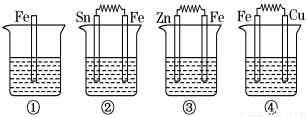
 ③②④①
③②④① 、SO
、SO B.Ca2+、H+、SO
B.Ca2+、H+、SO

 CH3OH(g)+ H2O(g) △H<0。CH3OH的浓度随时间变化如图,下列说法不正确的是
CH3OH(g)+ H2O(g) △H<0。CH3OH的浓度随时间变化如图,下列说法不正确的是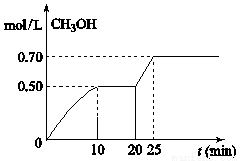

 xC(g) △H<0;在2min时达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写列空白:
xC(g) △H<0;在2min时达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写列空白: