题目内容
10.把180mL 2mol/L的H2SO4跟过量锌粉反应,在一定温度下,为了加快反应速率而不影响生成H2的总量,下列措施可行的是( )| A. | 改用20mL 18mol/L的H2SO4实验 | B. | 反应物中加入少量的硝酸钠固体 | ||
| C. | 反应物中加入少量的硫酸铜固体 | D. | 反应物中加入少量的碳酸钠固体 |
分析 过量的锌粉反应,硫酸完全反应,为了加快反应速率但又不影响生成氢气的总量,可增大氢离子浓度但不改变其物质的量,以此来解答.
解答 解:A、改用20mL 18mol/L的H2SO4实验,浓的硫酸和金属锌反不会产生氢气,故A错误;
B、反应物硫酸中加入少量的硝酸钠固体,会产生硝酸,硝酸和金属锌反不会产生氢气,故B错误;
C、反应物中加入少量的硫酸铜会和金属锌反应产生金属铜,构成原电池,加快反应速率,但是氢离子物质的量不变,所以不影响生成H2的总量,故C正确;
D、反应物中加入少量的碳酸钠回合硫酸中的氢离子之间反应产生二氧化碳,会减少氢气的量,故D错误.
故选C.
点评 本题考查影响化学反应速率的因素,为高频考点,注意信息中Zn过量及浓度对反应速率的影响即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
20.海带中提取碘的实验方法:
①称取3g干海带,用刷子把干海带表面的附着物刷净.
②将海带剪碎,用酒精润湿(便于灼烧)后,放在坩埚中.
③用酒精灯灼烧盛有海带的坩埚,至海带完全成灰,停止加热,冷却.
④将海带灰转移到小烧杯中,再向烧杯中加入10mL蒸馏水,搅拌,煮沸2~3min,使可溶物溶解,过滤.
⑤向滤液中滴入几滴硫酸,再加入约1mL H2O2溶液,观察现象.
下列说法正确的是( )
①称取3g干海带,用刷子把干海带表面的附着物刷净.
②将海带剪碎,用酒精润湿(便于灼烧)后,放在坩埚中.
③用酒精灯灼烧盛有海带的坩埚,至海带完全成灰,停止加热,冷却.
④将海带灰转移到小烧杯中,再向烧杯中加入10mL蒸馏水,搅拌,煮沸2~3min,使可溶物溶解,过滤.
⑤向滤液中滴入几滴硫酸,再加入约1mL H2O2溶液,观察现象.
下列说法正确的是( )
| A. | 步骤①中也可以用水洗涤除去海带表面的附着物 | |
| B. | 步骤④过滤操作需要两种玻璃仪器 | |
| C. | 步骤⑤所得的溶液中加入淀粉可看到蓝色现象 | |
| D. | 通过以上①~⑤步骤即可得到纯度高的I2 |
18.下列关于卤代烃的说法中正确的是( )
| A. | 所有卤代烃都是难溶于水、密度比水小的液体 | |
| B. | 所有卤代烃在常温下都是液体,且都是非电解质 | |
| C. | 所有卤代烃都含有卤原子 | |
| D. | 所有卤代烃都是通过取代反应制得的 |
2.下列说法不正确的是( )
| A. | 化学反应中的能量变化都表现为热量的变化 | |
| B. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 | |
| C. | 反应物的总能量低于生成物的总能量时,发生吸热反应 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
19.0.1mol•L-1的下列溶液:①HCl ②H2SO4③CH3COOH ④NaOH,水的电离程度由大到小的顺序正确的是( )
| A. | ③>①>②>④ | B. | ④>③>①>② | C. | ③>①=④>② | D. | ①=③=④>② |
20.一定条件下将总质量为Xg的混合物在足量氧气中完全燃烧,燃烧后全部产物通过足量过氧化钠层,过氧化钠层增重Yg,下列一定正确的是( )
| 选项 | 混合物 | X | Y |
| ① | C3H6、C2H4 | m | 15m/7 |
| ② | HCHO、HCOOH | m | 15m/23 |
| ③ | CH3OH、CH3COOH | m | m |
| ④ | HCOOH、CH3COOCH3 | m | m |
| A. | ①② | B. | ③② | C. | ①③ | D. | ③④ |
 .
.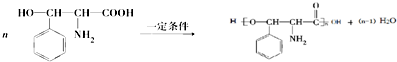 .
.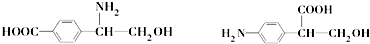

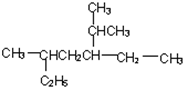 2,5-二甲基-3-乙基-庚烷
2,5-二甲基-3-乙基-庚烷 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$ .
.