题目内容
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子.根据以上叙述,下列说法中正确的是( )
| A.上述四种元素的原子半径大小为W<X<Y<Z |
| B.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| C.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
| D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
X的一种核素在考古时常用来鉴定一些文物的年代,用的是C14,采用的是断代法;工业上采用液态空气分馏方法来生产Y的单质,这是工业上生产氮的方法,因为X、Y、Z同族,Z的原子序数大于X、Y,且不能形成双原子,所以只能是稀有气体Ne,X、Y、Z核外内层电子是2个,所以W是H,则
A.X为C,Y为N,同周期元素从左到右元素的原子半径逐渐减小,则原子半径C>N,Z为Ne,原子半径测定依据不同,一般不与主族元素的原子半径相比较,故A错误;
B.W、X、Y、Z原子的核外最外层电子数的总和为1+4+5+8=18,故B错误;
C.W与Y可形成N2H4的化合物,既含极性共价键又含非极性共价键,故D正确;
D.W为H元素,X为C元素,Y为N元素,C和H可形成多种烃类化合物,当相对分子质量较大时,形成的烃在常温下为液体或固体,沸点较高,故C错误.
故选C.
A.X为C,Y为N,同周期元素从左到右元素的原子半径逐渐减小,则原子半径C>N,Z为Ne,原子半径测定依据不同,一般不与主族元素的原子半径相比较,故A错误;
B.W、X、Y、Z原子的核外最外层电子数的总和为1+4+5+8=18,故B错误;
C.W与Y可形成N2H4的化合物,既含极性共价键又含非极性共价键,故D正确;
D.W为H元素,X为C元素,Y为N元素,C和H可形成多种烃类化合物,当相对分子质量较大时,形成的烃在常温下为液体或固体,沸点较高,故C错误.
故选C.

练习册系列答案
相关题目
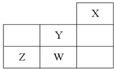 短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中不正确的是( )
短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中不正确的是( )| A、X元素形成的单质中存在非极性共价键 | B、W的最高价氧化物对应的水化物是强酸 | C、Y的原子半径在同周期主族元素中最小 | D、Z的气态氢化物的稳定性在同主族元素中最强 |
