题目内容
 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2的变化的曲线是
(3)能使该反应的反应速率增大的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂.
考点:化学平衡建立的过程,化学反应速率的影响因素,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)根据图结合表中的数据可知,图中c线为NO的变化曲线,因为在起点NO的物质的量为0.02mol,容器体积是2L,起始浓度为0.01mol/L,图中c线符合,在A点处,NO的物质的量浓度在减小,说明反应在向正反应方向进行,此时v(正)>v(逆),随着的时间的推移,反应物浓度下降,正反应速率下降,所以A点正反应速率 大于B点正反应速率,据此答题;
(2)NO2是生成物,浓度从0开始,根据化学方程式中NO与NO2的计量数相等,最终平衡时NO2的浓度小于0.01mol/L,所以表示NO2的浓度变化的曲线是b线,根据v=
求得NO的反应速率,再根据速率之比等于计量数之比计算O2的平均速率;
(3)根据影响化学反应速率的因素判断;
(2)NO2是生成物,浓度从0开始,根据化学方程式中NO与NO2的计量数相等,最终平衡时NO2的浓度小于0.01mol/L,所以表示NO2的浓度变化的曲线是b线,根据v=
| △c |
| t |
(3)根据影响化学反应速率的因素判断;
解答:
解:(1)根据图结合表中的数据可知,图中c线为NO的变化曲线,因为在起点NO的物质的量为0.02mol,容器体积是2L,起始浓度为0.01mol/L,图中c线符合,在A点处,NO的物质的量浓度在减小,说明反应在向正反应方向进行,此时v(正)>v(逆),随着的时间的推移,反应物浓度下降,正反应速率下降,所以A点正反应速率 大于B点正反应速率,故答案为:大于;大于;
(2)NO2是生成物,浓度从0开始,根据化学方程式中NO与NO2的计量数相等,反应中浓度的变化量也相等,最终平衡时NO2的浓度小于0.01mol/L,所以表示NO2的浓度变化的曲线是b线,根据v=
求得NO的反应速率为
mol/(L?s)=0.003mol/(L?s),再根据速率之比等于计量数之比计算O2的平均速率为
×0.003mol/(L?s)=0.0015mol/(L?s),故答案为:b;0.0015mol/(L?s);
(3)根据影响化学反应速率的因素判断,
a.及时分离出NO2气体,生成物浓度减小,平衡正向移动,反应物浓度也减小,所以正逆反应速率都减小;
b.适当升高温度,加快反应速率;
c.增大O2的浓度,平衡正向移动,生成物浓度增加,正逆反应速率都会加快;
d.选择高效的催化剂,可以同等程度提高正逆反应速率;
故选bcd.
(2)NO2是生成物,浓度从0开始,根据化学方程式中NO与NO2的计量数相等,反应中浓度的变化量也相等,最终平衡时NO2的浓度小于0.01mol/L,所以表示NO2的浓度变化的曲线是b线,根据v=
| △c |
| t |
| ||
| 2 |
| 1 |
| 2 |
(3)根据影响化学反应速率的因素判断,
a.及时分离出NO2气体,生成物浓度减小,平衡正向移动,反应物浓度也减小,所以正逆反应速率都减小;
b.适当升高温度,加快反应速率;
c.增大O2的浓度,平衡正向移动,生成物浓度增加,正逆反应速率都会加快;
d.选择高效的催化剂,可以同等程度提高正逆反应速率;
故选bcd.
点评:本题主要考查了化学反应速率的计算、影响化学反应速率的因素等知识点,中等难度,解题时注意基础知识的灵活运用.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、CO2通入Na2SiO3溶液中可以得到硅酸 |
| B、因为高温时SiO2与Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 |
| C、SiO2是酸性氧化物,它不溶于水也水溶于任何酸 |
| D、在制玻璃、制水泥的工业生产中,都需要的原料之一是石灰石 |
 密闭容器中发生下列反应:N2+3H2?2NH3△H<0,如图是某一时间段中反应速率与反应进程的曲线关系图.回答下列问题:
密闭容器中发生下列反应:N2+3H2?2NH3△H<0,如图是某一时间段中反应速率与反应进程的曲线关系图.回答下列问题: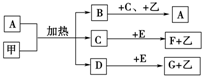 已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为短周期元素,A的浓溶液与甲能发生如图所示的反应,甲是常见的固体单质,乙是常见的气体单质,B是无色气体,是主要的大气污染物之一,请根据图示回答问题.
已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为短周期元素,A的浓溶液与甲能发生如图所示的反应,甲是常见的固体单质,乙是常见的气体单质,B是无色气体,是主要的大气污染物之一,请根据图示回答问题.
 某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.