��Ŀ����
һ���¶��£��ڹ̶��ݻ������Ϊ2L���ܱ������г���1molN2��3molH2������Ӧ������Ӧ���е�10sĩʱ�ﵽƽ�⣬��ʱ������c(NH3)=0.15mol��L-1�������й��жϲ���ȷ����
A����Ӧ��ƽ��ʱN2��ת����Ϊ7.5%
B����Ӧ���е�10sĩʱ��H2��ƽ����Ӧ������0.0225mol��(L��s)-1
C���÷�Ӧ�ﵽƽ��ʱ�ı�־�������������ܶȲ��ٸı�
D�������������г���1molN2��3molH2�����´ﵽƽ��ʱc(NH3)=0.30mol/L
��ϰ��ϵ�д�
 �ʰ�Ӣ��ͬ����ϰ��ϵ�д�
�ʰ�Ӣ��ͬ����ϰ��ϵ�д� ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д�
�����Ŀ
18���������ʵķ�����ȫ����ȷ���ǣ�������
| A�� | SiO2���������� Na2O���������� A12O3���������� | |
| B�� | ˮ����-����� ��ˮ�����-������ HT-���� | |
| C�� | ���-�� ʯ̿��-���� С�մ�-��ʽ�� | |
| D�� | ��ˮ-ǿ����� ���ᱵ-ǿ����� ����-������� |
15�����ж�������;�������У�������ǣ�������
| A�� | ��Mg��Al�Ƚϣ�þ���Ͻ��ǿ�Ⱥ�Ӳ�Ⱦ��ϴ������������IJ��� | |
| B�� | Cl2��SO2��NaClO��������Ư��ijЩ���� | |
| C�� | Ũ���������ˮ�ԣ������ڸ���HCl��H2S��O2 | |
| D�� | ̼���ƿ������������Ʋ��� |



 2AB3(g) ��H<0 ,������ͼ����ȷ����
2AB3(g) ��H<0 ,������ͼ����ȷ����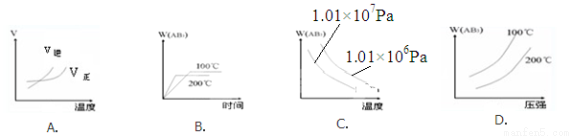
 zC(g)ƽ��ʱ���A��Ũ��Ϊ0.50mol/L�������¶Ȳ��䣬������������������������A��Ũ�ȱ�Ϊ0.3mol/L�������й��ж���ȷ����
zC(g)ƽ��ʱ���A��Ũ��Ϊ0.50mol/L�������¶Ȳ��䣬������������������������A��Ũ�ȱ�Ϊ0.3mol/L�������й��ж���ȷ����