题目内容
4.下列有关SO2和CO2的说法正确的是( )| A. | 都是非极性分子 | B. | 中心原子都采取sp杂化 | ||
| C. | S原子和C原子都没有孤对电子 | D. | SO2为V形结构,CO2为直线形结构 |
分析 二氧化碳中C原子价层电子对个数=2+$\frac{4-2×2}{2}$=2,所以采用sp杂化,直线形结构,是非极性分子;二氧化硫分子中S原子价层电子对个数=2+$\frac{6-2×2}{2}$=3,所以采用sp2杂化,V形结构,是极性分子,以此来解答.
解答 解:A.CO2是非极性分子,故A错误;
B.二氧化硫分子中S原子价层电子对个数=2+$\frac{6-2×2}{2}$=3,所以采用sp2杂化,二氧化碳中C原子价层电子对个数=2+$\frac{4-2×2}{2}$=2,所以采用sp杂化,故B错误;
C.S原子有一个孤对电子,C原子没有孤对电子,故C错误;
D.SO2采用sp2杂化,为V形结构,CO2采用sp杂化,为直线形结构,故D正确;
故选D.
点评 本题主要考查了原子的杂化,分子构型、分子的极性,难度不大,注意杂化方式的确定.

练习册系列答案
相关题目
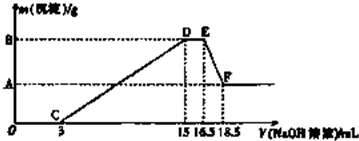
14.手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,下图是利用手持技术得到的微粒物质的量变化图,常温下向20ml0.2mol/LH2A溶液中滴加0.2mol/LNaOH溶液.下列说法正确的是( )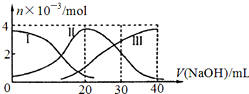

| A. | H2 A在水中的电离方程式是:H2A=H ++HA -;HA -═H++A2- | |
| B. | 当V(NaOH)=20mL时,则有:c(Na + )>c(HA- )>c(H + )>c(A 2- )>c(OH- ) | |
| C. | 当V(NaOH)=30mL时,则有:2c(H + )+c(HA- )+2c(H2A)=c(A 2- )+2 c(OH- ) | |
| D. | 当V(NaOH)=40mL时,其溶液中水的电离受到抑制 |
9.分子式为C8H16的某烯烃氢化后得到的饱和烃是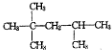 ,则该烯烃的结构最多有( )
,则该烯烃的结构最多有( )
 ,则该烯烃的结构最多有( )
,则该烯烃的结构最多有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
13.下列离子方程式书写正确的是( )
| A. | 向CuSO4溶液中加入钠:2Na+Cu2+=Cu+2Na+ | |
| B. | 向Ba(OH)2溶液中滴加稀盐酸:2H++2Cl-+Ba2++2OH-=2H2O+BaCl2 | |
| C. | 澄清石灰水与盐酸反应:H++OH-=H2O | |
| D. | Na2O2与水发生反应:2O22-+2 H2O=4 OH-+O2↑ |
 、
、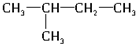 .
.
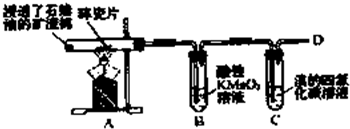 乙烯是石油裂解气的主要成分,下图是石蜡油在炽热碎瓷片的作用下裂解,下列装置检验其性质,完成下列问题.
乙烯是石油裂解气的主要成分,下图是石蜡油在炽热碎瓷片的作用下裂解,下列装置检验其性质,完成下列问题.