题目内容
12.配平下列各氧化还原反应方程式(将系数填写在相应横线上,并按要求填空)(1)2 KMnO4+16 HCl═2 MnCl2+2 KCl+5 Cl2↑+8 H2O
(2)4 HNO3═4NO2↑+1 O2↑+2H2O.
分析 (1)反应中KMnO4+→MnCl2,Mn元素化合价由+7降低为+2,共降低5价,Cl(浓)→Cl2,Cl元素化合价由-1价升高为0价,共升高为2价,化合价升降最小公倍数为10,故KMnO4的系数为2,Cl2的系数为5,再根据原子守恒配平其它物质的系数;
(2)反应中硝酸既做氧化剂又做还原剂,N元素化合价由+5价降低为+4价,O元素由-2价升高到0价,化合价升降最小公倍数为2,又由于氧气为双原子分子,故NO2的系数为4,O2的系数为1,再根据原子守恒配平其它物质的系数.
解答 解:(1)反应中KMnO4+→MnCl2,Mn元素化合价由+7降低为+2,共降低5价,Cl(浓)→Cl2,Cl元素化合价由-1价升高为0价,共升高为2价,化合价升降最小公倍数为10,故KMnO4的系数为2,Cl2的系数为5,再根据原子守恒配平其它物质的系数,配平后的化学方程式为:2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O,
故答案为:2;16;2;2;5;8;
(2)反应中硝酸既做氧化剂又做还原剂,N元素化合价由+5价降低为+4价,O元素由-2价升高到0价,化合价升降最小公倍数为2,又由于氧气为双原子分子,故NO2的系数为4,O2的系数为1,再根据原子守恒配平其它物质的系数,配平后的化学方程式为:4HNO3=4NO2↑+O2↑+H2O,
故答案为:4;4;1;2.
点评 本题考查了氧化还原反应的配平,题目难度不大,明确氧化还原反应的特征为解答关键,注意掌握化合价升降法在配平氧化还原反应中的应用,试题培养了学生的灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列过程中不涉及氧化还原反应的是( )
| A. | 用葡萄酿制葡萄酒 | |
| B. | 夏季油脂变质 | |
| C. | 烹鱼时加入少量的料酒和食醋可减少腥味,增加香味 | |
| D. | 用新制氢氧化铜悬浊液检验病人是否患糖尿病 |
3.某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有大烧杯、两个小烧杯、50mL量筒两个、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1盐酸、0.55mol•L-1 NaOH溶液,实验尚缺少的玻璃用品是温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”).
(3)他们记录的实验数据如下:
已知:Q=c•m•(t2-t1),反应后溶液的比热容c为4.18J•℃-1•g-1,各物质的密度均为1g•cm-3.
计算完成上表中△H=-56.8kJ/mol(保留到小数点后一位),中和热数值偏小的原因可能是分多次把NaOH溶液倒人盛有HCl小烧杯中(任填一条即可).
(4)若用KOH代替NaOH做实验,测定结果中和热数值无(填“有”或“无”)影响;若用醋酸代替HCl做实验,测定结果中和热数值偏小(填“偏大”、“偏小”或“无影响”).
(1)实验桌上备有大烧杯、两个小烧杯、50mL量筒两个、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1盐酸、0.55mol•L-1 NaOH溶液,实验尚缺少的玻璃用品是温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”).
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.5℃ | |
计算完成上表中△H=-56.8kJ/mol(保留到小数点后一位),中和热数值偏小的原因可能是分多次把NaOH溶液倒人盛有HCl小烧杯中(任填一条即可).
(4)若用KOH代替NaOH做实验,测定结果中和热数值无(填“有”或“无”)影响;若用醋酸代替HCl做实验,测定结果中和热数值偏小(填“偏大”、“偏小”或“无影响”).
17.根据所学规律,你认为下列物质在水中溶解度较大的是( )
| A. | 甲烷 | B. | 二氧化碳 | C. | 二氧化硫 | D. | 氢气 |
4.1-丙醇蒸气与空气混合通过加热的铜网,生成一种化合物,与该化合物互为同分异构体的是( )
①CH3CH2OCH3
②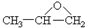
③CH3OOCCH3
④CH3COCH3
⑤CH3CHOHCH3.
①CH3CH2OCH3
②

③CH3OOCCH3
④CH3COCH3
⑤CH3CHOHCH3.
| A. | ①③ | B. | ①⑤ | C. | ②④ | D. | ①④ |
1.元素性质呈现周期性变化的本质原因是( )
| A. | 相对原子质量逐渐增大 | B. | 原子核外电子排布呈现周期性变化 | ||
| C. | 核电荷数逐渐增大 | D. | 元素的化合价呈现周期性变化 |
2.在下列过程中,浓硫酸既表现强氧化性,又表现强酸性的是( )
| A. | 用浓硫酸做干燥剂 | |
| B. | 将火柴梗插入浓硫酸中,火柴梗很快变黑 | |
| C. | 铜与浓硫酸加热时发生反应 | |
| D. | 锌与稀硫酸发生置换反应制取氢气 |
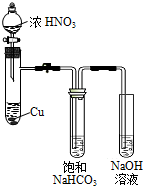 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应: