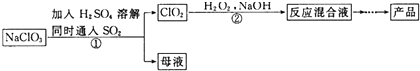
题目内容
3.现有五种有机物:乙烯、乙醇、乙酸、乙酸乙酯、苯.(1)请分别写出其中含有以下官能团的有机物的名称:
①醇羟基乙醇;
②-COOH乙酸.
(2)在上述四种有机物中,(填写有机物的结构简式)
①既能发生加成反应,又能发生聚合反应的是乙烯.
②能发生水解反应的是乙酸乙酯.
(3)把苯加入到盛有溴水的试管中,液体会出现分层现象,充分震荡、静置,出现橙红色液体的一层在上层(填“上”或“下”).
分析 (1)①醇中含有醇羟基;
②羧酸中含有羧基;
(2)①含有碳碳不饱和键的有机物能发生加成反应、加聚反应;
②含有酯基、肽键或卤原子的有机物能发生水解反应;
(3)苯和水不互溶且密度小于水,溴在水中的溶解度小于在苯中的溶解度,所以苯能萃取溴水中的溴而使苯呈橙色.
解答 解:(1)①醇中含有醇羟基,所以乙醇中含有醇羟基,故答案为:乙醇;
②羧酸中含有羧基,乙酸中含有羧基,故答案为:乙酸;
(2)①含有碳碳不饱和键的有机物能发生加成反应、加聚反应,乙烯中含有碳碳双键,所以能发生加成反应、加聚反应,故答案为:乙烯;
②含有酯基、肽键或卤原子的有机物能发生水解反应,乙酸乙酯中含有酯基,所以能发生水解反应,故答案为:乙酸乙酯;
(3)苯和水不互溶且密度小于水,溴在水中的溶解度小于在苯中的溶解度,所以苯能萃取溴水中的溴而使苯呈橙色,苯和水混合时苯在上层,所以苯萃取溴水中的溴后,苯层在上层,故答案为:上.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,知道萃取剂的选取方法,题目难度不大.

练习册系列答案
相关题目
13.根据元素周期律及元素周期表的知识分析,下列关系中不正确的是( )
| A. | 酸性强弱:H3PO4>H2SO4>HClO4 | B. | 离子半径大小:F->Na+>Mg2+>Al3+ | ||
| C. | 稳定性大小:SiH4<PH3<H2S<HCl | D. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 |
14.下列实验方案能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有 乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液, 加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 证明HCOOH结构中含有醛 基 | 将1mL 1mol/L HCOOH溶液加入装有银氨溶液 的试管中并水浴加热,观察有无银镜产生 |
| C | 除去甲烷中的乙烯 | 将混合气通入KMnO4溶液中洗气 |
| D | 制取乙烯气体 | 将无水乙醇和浓硫酸混合加热到140℃ |
| A. | A | B. | B | C. | C | D. | D |
11.有关该物质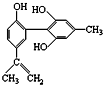 的说法正确的是( )
的说法正确的是( )
 的说法正确的是( )
的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 该分子中的所有碳原子不可能共平面 | |
| C. | 滴入酸性KMnO4溶液,观察紫色褪去,能证明结构中存在碳碳双键 | |
| D. | 1 mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别为4 mol、7 mol |
8.同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2,进行喷泉实验.经充分反应后,瓶内溶质的物质的量浓度为,假设溶质不扩散( )
| A. | ①=② | B. | ①<② | C. | ①>② | D. | 不能确定 |
15.下列叙述正确的是( )
| A. | H2O的摩尔质量为18g | |
| B. | 3.01×1023个SO2分子的质量为32g | |
| C. | 标准状况下,1 mol任何物质体积均为22.4L | |
| D. | 将0.1mol NH3溶于1L水,配成溶液中溶质的物质的量浓度为0.1mol/L |
12.欲除去Cl2中的少量HCl气体,可选用( )
| A. | NaOH溶液 | B. | AgNO3溶液 | C. | 饱和食盐水 | D. | 石灰水 |
11.下列说法正确的是( )
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 船体镀锌或锡均可保护船体,镀层破损后将立即失去保护作用 | |
| C. | 由于共价键具有方向性,共价化合物在形成晶体时均采取“紧密堆积” | |
| D. | 反应NH4Cl (s)═NH3(g)+HCl(g)室温下不能自发进行,则该反应的△H>0 |