题目内容
可逆反应①X(g)+2Y(g )?2Z(g)、②2M(g)?N(g)+p(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦,可滑动的密封隔板.反应开始和达到平衡状态时有关物理量的变化如图所示:
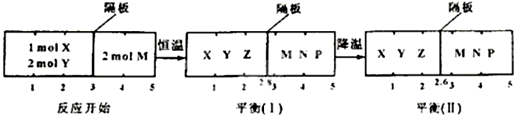
填写下列空白:
(1)反应①的正反应是 反应,(填“吸热”或“放热”)理由是
(2)平衡(I)与平衡(II)体系的总物质的量之比为
(3)平衡(II)时X的转化率为 ,Y的转化率为
(4)若反应②的△H<0,在平衡(I)和平衡(II)中,M的体积分数较大的是
(5)若只改变温度,隔板能否移至2.5处 (填“能”或“否”),原因是: .

填写下列空白:
(1)反应①的正反应是
(2)平衡(I)与平衡(II)体系的总物质的量之比为
(3)平衡(II)时X的转化率为
(4)若反应②的△H<0,在平衡(I)和平衡(II)中,M的体积分数较大的是
(5)若只改变温度,隔板能否移至2.5处
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)根据右室的混合物总物质的量不变,平衡(I)、平衡(Ⅱ)左右两室的温度、压强相同,体积之比等于物质的量之比,结合图示容器容积变化判断降温后反应①平衡移动的方向;
(2)根据右室的混合物总物质的量不变,在同温同压下体积比等于物质的量之比计算出反应后(I)和(II)中左室混合气体的物质的量,再计算出达平衡(I)和(II)时总物质的量;
(3)设参加反应的X的物质的量为amol,利用差量法计算a的值,再利用转化率定义计算X、Y的转化率;
(4)根据右边反应2M(g)?N(g)+P(g)气体的总物质的量不变,温度变化结合△H<0,通过平衡移动来判断;
(5)假如隔板能移至2.5处,则根据左右两室的压强、温度相等,同温同压下,体积之比等于物质的量之比,平衡左室混合气体总的物质的量也为2mol,则X和Y全部转化成Z,又可逆反应不可能完全反应到底,故不可能.
(2)根据右室的混合物总物质的量不变,在同温同压下体积比等于物质的量之比计算出反应后(I)和(II)中左室混合气体的物质的量,再计算出达平衡(I)和(II)时总物质的量;
(3)设参加反应的X的物质的量为amol,利用差量法计算a的值,再利用转化率定义计算X、Y的转化率;
(4)根据右边反应2M(g)?N(g)+P(g)气体的总物质的量不变,温度变化结合△H<0,通过平衡移动来判断;
(5)假如隔板能移至2.5处,则根据左右两室的压强、温度相等,同温同压下,体积之比等于物质的量之比,平衡左室混合气体总的物质的量也为2mol,则X和Y全部转化成Z,又可逆反应不可能完全反应到底,故不可能.
解答:
解:(1)右室的混合物总物质的量不变,平衡(I)、平衡(Ⅱ)左右两室的温度、压强相同,体积之比等于物质的量之比,由图可知,平衡(I)降低温度达新平衡平衡(Ⅱ),隔板由2.8处移至2.6处,左室的气体的物质的量减小,降低温度平衡向正反应移动,降低温度平衡向放热反应移动,故该反应正反应为放热反应,
故答案为:放热;降温隔板由2.8处移至2.6处,左室的气体的物质的量减小,即平衡向正反应移动,所以该反应正反应为放热反应;
(2)平衡(I)时右室的混合物总物质的量不变为2mol,左右两室的压强、温度相等,同温同压下,体积之比等于物质的量之比,平衡(I)中左室混合气体总的物质的量为
×2mol=
mol;同理平衡(II)时右室的混合物总物质的量不变为2mol,左右两室的压强、温度相等,同温同压下,体积之比等于物质的量之比,平衡(II)中左室混合气体总的物质的量为
×2mol=
mol,所以平衡(I)与平衡(II)体系的总物质的量之比为
=12:11,
故答案为:12:11;
(3)根据(2)可知,平衡(II)中左室混合气体总的物质的量为
mol,设参加反应的X的物质的量为amol,则:
X(g)+2Y(g)?2Z(g) 物质的量减少△n
1 2 1
amol 2a (3mol-
mol)=
mol
解得a=
mol,所以X的转化率为
=
,Y的转化率为
=a=
故答案为:
;
;
(4)右室中气体的总物质的量始终不变,但是由于降低温度,则反应②的△H<0,反应2M(g)?N(g)+P(g)的平衡向正反应方向移动,导致M的含量降低,所以M的体积分数较大的是平衡(I)
故答案为:平衡(I);
(5)假如隔板能移至2.5处,则根据左右两室的压强、温度相等,同温同压下,体积之比等于物质的量之比,平衡左室混合气体总的物质的量也为2mol,则X和Y全部转化成Z,又可逆反应不可能完全反应到底,故不可能;
故答案为:否;可逆反应不能进行彻底;
故答案为:放热;降温隔板由2.8处移至2.6处,左室的气体的物质的量减小,即平衡向正反应移动,所以该反应正反应为放热反应;
(2)平衡(I)时右室的混合物总物质的量不变为2mol,左右两室的压强、温度相等,同温同压下,体积之比等于物质的量之比,平衡(I)中左室混合气体总的物质的量为
| 2.8 |
| 2.2 |
| 28 |
| 11 |
| 2.6 |
| 2.4 |
| 13 |
| 6 |
| ||
|
故答案为:12:11;
(3)根据(2)可知,平衡(II)中左室混合气体总的物质的量为
| 13 |
| 6 |
X(g)+2Y(g)?2Z(g) 物质的量减少△n
1 2 1
amol 2a (3mol-
| 13 |
| 6 |
| 5 |
| 6 |
解得a=
| 5 |
| 6 |
| ||
| 1 |
| 5 |
| 6 |
| 2a |
| 2 |
| 5 |
| 6 |
故答案为:
| 5 |
| 6 |
| 5 |
| 6 |
(4)右室中气体的总物质的量始终不变,但是由于降低温度,则反应②的△H<0,反应2M(g)?N(g)+P(g)的平衡向正反应方向移动,导致M的含量降低,所以M的体积分数较大的是平衡(I)
故答案为:平衡(I);
(5)假如隔板能移至2.5处,则根据左右两室的压强、温度相等,同温同压下,体积之比等于物质的量之比,平衡左室混合气体总的物质的量也为2mol,则X和Y全部转化成Z,又可逆反应不可能完全反应到底,故不可能;
故答案为:否;可逆反应不能进行彻底;
点评:本题考查化学平衡移动与化学计算,题目难度中等,是对知识的综合运用,需要学生具备扎实的基础知识与运用知识分析问题、解决问题的能力,平衡( I)和( II)中清楚左右两室的温度、压强相同,体积之比等于物质的量之比是解题关键.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A、22.4L(标况下)NO与0.5molO2混合充分反应,最后得到NA个NO2分子 |
| B、任何反应中,生成1molO2都转移4NA个电子 |
| C、100g17%的氨水,溶液中含有氨气分子NA |
| D、7.1gCl2与足量氢氧化钠溶液反应转移电子数为0.1NA |
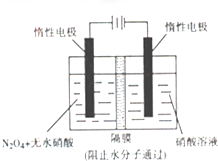

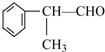
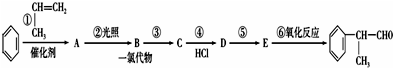

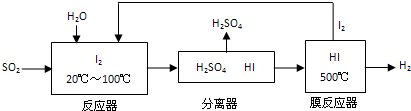
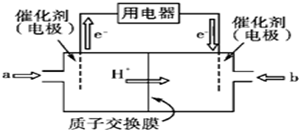
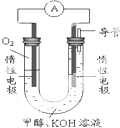 甲醇(CH3OH)是一种可再生能源,具有广泛的开发和应用前景.
甲醇(CH3OH)是一种可再生能源,具有广泛的开发和应用前景.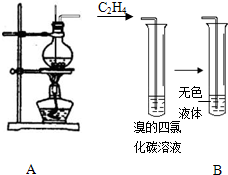 某学习小组用如图所示装置进行验证乙醇和浓硫酸混合加热后是否有乙烯生成的实验.
某学习小组用如图所示装置进行验证乙醇和浓硫酸混合加热后是否有乙烯生成的实验.