题目内容
(10 分)游泳池水的含氯气量应该控制在0.5mg/L至1.0 mg /L之间,

(1)写出氯气溶于水后的化学方程式 。
(2)你认为哪几天的天气炎热、阳光强烈 ,理由是 。(用化学方程式表示)
(3)小型泳池通常使用次氯酸钠溶液而非氯气来消毒池水,试举出使用次氯酸钠溶液而非氯气的一项理由 。用化学方程式说明工业上如何生产次氯酸钠溶液 。
(1)Cl2 + H2O = HCl + HClO(2分);(2)星期六、星期日(2分);2HClO 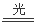 2HCl+ O2。(2分)
2HCl+ O2。(2分)
(3)次氯酸钠溶液比较稳定,容易储运。(2分) ;Cl2 + 2NaOH = NaClO + NaCl + H2O (2分)。
【解析】
试题分析:(1)写出氯气溶于水后的化学方程式是Cl2 + H2O = HCl + HClO;(2)根据图表可知:你认为哪几天的天气炎热、阳光强烈是星期六、星期日,原因是温度高HClO分解,产生氧气,所以Cl的含量高,方程式表示是2HClO  2HCl+ O2。(3)小型泳池通常使用次氯酸钠溶液而非氯气来消毒池水,试举出使用次氯酸钠溶液而非氯气的一项理由是次氯酸钠溶液比较稳定,容易储运。用化学方程式表示生产次氯酸钠溶液的反应是Cl2 + 2NaOH = NaClO + NaCl + H2O。
2HCl+ O2。(3)小型泳池通常使用次氯酸钠溶液而非氯气来消毒池水,试举出使用次氯酸钠溶液而非氯气的一项理由是次氯酸钠溶液比较稳定,容易储运。用化学方程式表示生产次氯酸钠溶液的反应是Cl2 + 2NaOH = NaClO + NaCl + H2O。
考点:考查氯气的单质及化合物的性质及应用的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列实验“操作和现象”与“结论”对应关系正确的是
| 操作和现象 | 结论 |
A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
C | 向饱和Na2CO3溶液中通入足量CO2 ,溶液变浑浊 | 析出了NaHCO3 |
D | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
 、
、