题目内容
20.F、G都是常见的高分子材料,以下是由丙烯合成F、G的流程图.
(1)E的化学名称是2-羟基丙酸,所含官能团是羧基、羟基.
(2)G的结构简式是
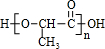 .
.(3)A→B的化学方程式是CH3CHBrCH2Br+2NaOH$→_{△}^{水}$CH3CH(OH)CH2OH+2NaBr,该反应类型是取代反应.
(4)由CH3CH=CH2生成F的化学方程式是nCH3CH=CH2$\stackrel{一定条件}{→}$
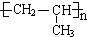 ,该反应类型是加聚反应.
,该反应类型是加聚反应.(5)在一定条件下,两分子E脱去两分子水形成一种六元环状化合物,该化合物的结构简式是
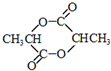 .
.(6)C的同分异构体有多种,请分别写出符合下列条件有机物的结构简式:
①能与NaHCO3溶液反应的是CH2=CHCOOH;
②能发生水解反应的是HCOOCH=CH2.
分析 丙烯与溴发生加成反应生成A为CH3CHBrCH2Br,A发生水解反应生成B为CH3CH(OH)CH2OH,B氧化生成C为 ,C进一步氧化生成D为
,C进一步氧化生成D为 ,D与氢气发生加成反应生成E为
,D与氢气发生加成反应生成E为 ,E发生缩聚反应生成G为
,E发生缩聚反应生成G为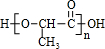 ,丙烯发生加聚反应生成F为
,丙烯发生加聚反应生成F为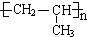 .
.
解答 解:丙烯与溴发生加成反应生成A为CH3CHBrCH2Br,A发生水解反应生成B为CH3CH(OH)CH2OH,B氧化生成C为 ,C进一步氧化生成D为
,C进一步氧化生成D为 ,D与氢气发生加成反应生成E为
,D与氢气发生加成反应生成E为 ,E发生缩聚反应生成G为
,E发生缩聚反应生成G为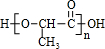 ,丙烯发生加聚反应生成F为
,丙烯发生加聚反应生成F为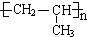 .
.
(1)E为 ,化学名称是2-羟基丙酸,所含官能团是羧基、羟基,故答案为:2-羟基丙酸;羧基、羟基;
,化学名称是2-羟基丙酸,所含官能团是羧基、羟基,故答案为:2-羟基丙酸;羧基、羟基;
(2)G的结构简式是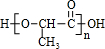 ,故答案为:
,故答案为: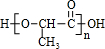 ;
;
(3)A→B的化学方程式是:CH3CHBrCH2Br+2NaOH$→_{△}^{水}$CH3CH(OH)CH2OH+2NaBr,属于取代反应,
故答案为:CH3CHBrCH2Br+2NaOH$→_{△}^{水}$CH3CH(OH)CH2OH+2NaBr;取代反应;
(4)由CH3CH=CH2生成F的化学方程式是:nCH3CH=CH2$\stackrel{一定条件}{→}$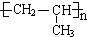 ,属于加聚反应,
,属于加聚反应,
故答案为:nCH3CH=CH2$\stackrel{一定条件}{→}$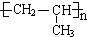 ,加聚反应;
,加聚反应;
(5)在一定条件下,两分子E脱去两分子水形成一种六元环状化合物,该化合物的结构简式是 ,故答案为:
,故答案为: ;
;
(6)C( )的同分异构体有多种,其中①能与NaHCO3溶液反应的是CH2=CHCOOH,②能发生水解反应的是:HCOOCH=CH2,故答案为:CH2=CHCOOH;HCOOCH=CH2.
)的同分异构体有多种,其中①能与NaHCO3溶液反应的是CH2=CHCOOH,②能发生水解反应的是:HCOOCH=CH2,故答案为:CH2=CHCOOH;HCOOCH=CH2.
点评 本题考查有机物推断,熟练掌握官能团的性质与转化,是对有机化学基础的综合考查,有利于基础知识的巩固.

练习册系列答案
相关题目
11.1L含氢气和1,3-丁二烯的混合气体,其中1,3丁二烯的体积百分含量为x%.在一定条件下充分反应后,恢复到原来的状态,所得气体的体积为y升.则下列关系式中正确的是( )
| A. | y=x%<$\frac{1}{2}$ | B. | y=1-x%>$\frac{2}{3}$ | C. | y=x%>$\frac{1}{3}$ | D. | y=1-2x%>$\frac{1}{3}$ |
15.NA为阿伏加德罗常数的值.下列说法中,正确的是( )
| A. | 常温常压下,l.6g${\;}_{6}^{14}$CH4中含有共价键总数为0.4NA | |
| B. | 密闭容器中2molNO与1molO2充分反应后,容器内气体的分子数为2NA | |
| C. | 1 L 0.lmol•L-1的CH3COONa溶液中CH3COO-和CH3COOH粒子数之和为0.1NA | |
| D. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA |
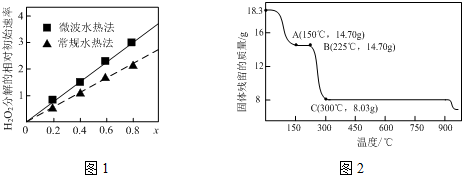

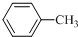 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$
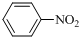 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$ (苯胺,易被氧气氧化)
(苯胺,易被氧气氧化) .
. .写出③的转化关系
.写出③的转化关系 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$ (用已知中的表达方式表示,不用写化学方程式).
(用已知中的表达方式表示,不用写化学方程式).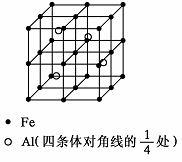 第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.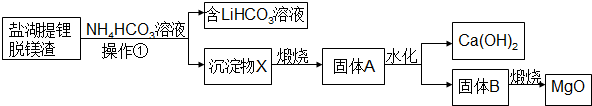
 .
. .
.