题目内容
17.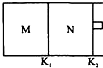 如图所示,隔板K1固定不动,活塞K2可自由移动.T℃时,M、N两个容器中均发生反应N2(g)+3H2(g)?2NH3(g),向容器M、N中各充入l mol N2和3mol H2,初始M、N的容积和温度相同,并保持温度不变.下列说法中不正确的是( )
如图所示,隔板K1固定不动,活塞K2可自由移动.T℃时,M、N两个容器中均发生反应N2(g)+3H2(g)?2NH3(g),向容器M、N中各充入l mol N2和3mol H2,初始M、N的容积和温度相同,并保持温度不变.下列说法中不正确的是( )| A. | 反应达到平衡时N2的转化率:M<N | B. | H2的体积分数:M<N | ||
| C. | NH3的浓度:M<N | D. | 该反应在T℃时的平衡常数K:M=N |
分析 M容器保持恒容,N容器保持恒压,由于N2(g)+3H2(g)?2NH3(g)中反应前后的气体系数和不等,所以两个平衡态也不一样,M容器达到平衡后气体压强减小,N容器中保持恒压,反应达到平衡过程中压强大于M容器,平衡正向进行;
A、M容器达到平衡后压强减小,N容器中保持恒压,反应达到平衡过程中N容器的压强大于M容器,平衡正向进行;
B、M容器达到平衡后体系压强减小,N容器中保持恒压,反应达到平衡过程中N的压强大于M容器,平衡正向进行;
C、M容器达到平衡后气体压强减小,N容器中保持恒压,反应达到平衡过程中压强大于M容器,平衡正向进行;
D、由于两个反应的温度相同,则两个反应的化学平衡常数相等.
解答 解:M容器保持恒容,N容器保持恒压,由于反应前后的气体系数和不等,所以两个平衡态也不一样,M容器达到平衡后压强减小,N容器中保持恒压,反应达到平衡过程中压强大于M容器,平衡正向进行;
A、M容器达到平衡后压强减小,N容器中保持恒压,反应达到平衡过程中N容器内的压强大于M容器,增大压强,平衡正向进行,所以达到平衡后氮气的转化率:M<N,故A正确;
B、M容器达到平衡后体系压强减小,N容器中保持恒压,反应达到平衡过程中N容器内气体的压强大于M容器,平衡正向进行,达到平衡后氢气的体积分数:M>N,故B错误;
C、M容器达到平衡后气体压强减小,N容器中保持恒压,反应达到平衡过程中压强大于M容器,平衡正向进行,容器M中氨气浓度小于N容器中氨气,NH3的浓度:M<N,故C正确;
D、M容器保持恒容,N容器保持恒压,由于反应前后的气体系数和不等,所以两个平衡态也不一样,但温度相同平衡常数相同,该反应在T℃时的平衡常数K:M=N,故D正确;
故选B.
点评 本题考查化学平衡的计算、平衡常数的计算等,题目难度较大,注意掌握化学平衡的影响因素、化学平衡常数的概念,选项C为难点,注意三段式在计算出中的应用方法.

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案| A. | 在Na2B溶液中一定有:c(OH-)=c(H+)+c(HB-)+2c(H2B) | |
| B. | NaHB溶液可能存在以下关系:c(Na+)>c(HB-)>c(OH-)>c(H+) | |
| C. | NaHB水溶液中一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+c(B2-) | |
| D. | NaHB溶液一定呈酸性,Na2B溶液一定呈碱性 |
| A. | 向某溶液中滴加NaOH溶液并加热,用湿润的蓝色石蕊试纸于试管口以检验NH4+ | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加入盐酸,沉淀不消失,一定有SO42- | |
| C. | 某待测液焰色反应呈黄色,则待测液中一定不含有K+ | |
| D. | 某溶液中加入KSCN后,溶液无变化,再加入H2O2后,溶液变成血红色,说明原溶液中一定含有Fe2+ |
| A. | 加入硝酸银溶液,有白色沉淀生成,证明一定有Cl-存在 | |
| B. | 加入BaCl2溶液和稀硝酸,有白色沉淀生成,证明一定有SO42- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加入盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH4+ |
| A. | 青铜 | B. | 钢 | C. | 硬铝 | D. | 玻璃 |
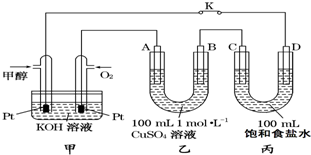 如图是甲醇(CH3OH)燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
如图是甲醇(CH3OH)燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.