题目内容
1.常温下,0.1mol/L的HA溶液与0.1mol/L的MOH溶液等体积混合后溶液显酸性,一定水解的离子方程式为M++H2O?MOH+H+.分析 常温下,0.1mol/L的HA溶液与0.1mol/L的MOH溶液等体积混合后溶液显酸性,酸碱恰好完全反应生成的盐中阳离子为弱碱阳离子水解.
解答 解:常温下,0.1mol/L的HA溶液与0.1mol/L的MOH溶液等体积混合,反应的孩子方程式为HA+MOH=MA+H2O,混合后溶液显酸性,说明酸碱恰好完全反应生成的盐中阳离子为弱碱阳离子水解,一定水解的离子方程式为:M++H2O?MOH+H+,
故答案为:M++H2O?MOH+H+.
点评 本题考查了盐类水解的原理、反应离子方程式书写,掌握基础是解题关键,题目难度不大.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
11.可用于判断溶液酸碱性的方法有很多,下列能够说明溶液一定呈碱性的是( )
| A. | 常温下能够使pH试纸显红色的溶液 | B. | 常温下能够使甲基橙显黄色的溶液 | ||
| C. | [OH-]>[H+]的溶液 | D. | 加入MgCl2生成白色沉淀的溶液 |
12.常温下,a、b、c三种溶液的pH如图,则c代表的溶液可能为( )
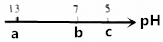
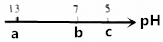
| A. | NaCl溶液 | B. | NaOH溶液 | C. | CH3COOK溶液 | D. | NH4Cl溶液 |
9.下列叙述正确的是( )
| A. | 过氧化钠与足量的CO2气体反应转移1mole-时增重的质量为28g | |
| B. | 碳酸钠的碱性较弱,可用作治疗胃酸过多的药物 | |
| C. | 生活中的“高钙牛奶”、“加铁酱油”中的钙和铁指的是钙离子和亚铁离子 | |
| D. | 氯化铝坩埚可用来熔融碳酸钠固体 |
16.下列离子方程式书写正确的是( )
| A. | 一定量Cl2通入FeBr2溶液中:5Cl2+4Fe2++6Br-═10Cl-+4Fe3++2Br2 | |
| B. | 过量CO2通入NaAlO2溶液中:CO2+3H2O+2AlO2-═2Al(OH)3↓+CO32- | |
| C. | 在溶液中NH4HSO3于NaOH等物质的量混合:NH4++HSO3-+2OH-═SO32-+NH3↑+2H2O | |
| D. | Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ |
13.波尔多液是果农常用的一种杀菌剂,氯吡苯脲是一种西瓜膨大剂(植物生长调节剂),其组成结构和物理性质见表.
回答下列问题:
(1)氯吡苯脲晶体中,氮原子的杂化轨道类型为sp3、sp2杂化.
(2)氯吡苯脲晶体中,微粒间的作用力类型有BCD.
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键.
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O |  | 白色结晶粉末 | 170~ 172℃ | 易溶 于水 |
(1)氯吡苯脲晶体中,氮原子的杂化轨道类型为sp3、sp2杂化.
(2)氯吡苯脲晶体中,微粒间的作用力类型有BCD.
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键.