题目内容
11.下列实验装置设计正确,且能达到目的是( )| A. |  测定乙醇分子结构 | B. | 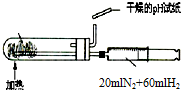 合成氨并检验氨的生成 | ||
| C. | 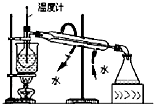 碘的CCl4溶液中分离I2 | D. | 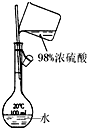 配制稀硫酸溶液 |
分析 A.利用生气气体的体积确定乙醇中-OH,从而确定结构式;
B.干燥的氨气不能使试纸变色;
C.温度计应测定蒸气的温度,其位置错误;
D.容量瓶不能溶解或稀释药品,只能配制一定物质的量浓度溶液.
解答 解:A.钠与乙醇反应生成氢气,利用生成气体的体积确定乙醇中-OH,从而确定结构式,故A正确;
B.在催化剂的作用下生成的氨气为干燥的气体,干燥的氨气不能使试纸变色,则不能说明氨气的生成,故B错误;
C.温度计应测定蒸气的温度,其位置应在蒸馏烧瓶的支管口处,故C错误;
D.容量瓶不能溶解或稀释药品,只能配制一定物质的量浓度溶液,应该在烧杯中稀释浓硫酸,冷却至室温后再转移到容量瓶中,故D错误;
故选A.
点评 本题考查实验方案的评价,涉及结构式的确定、气体的检验、物质的分离、溶液配制,注重对实验中的操作的考查,明确实验原理及基本操作方法是解本题关键,题目难度不大.

练习册系列答案
相关题目
1.氢氧化铝在水中可建立如下平衡:Al3++3OH-?Al(OH)3?H++AlO2-+H2O,运用勒夏特列原理判断,下列叙述中正确的是( )
| A. | 向以上平衡体系中加入足量浓NaOH溶液,两平衡都向右移动,Al(OH)3的质量增加 | |
| B. | 向以上平衡体系中加入足量浓盐酸,Al3+的物质的量增加 | |
| C. | 在同一溶液中,Al3+与OH-能大量共存 | |
| D. | 在同一溶液中,AlO2-与H+能大量共存 |
19.下列离子方程式中,只能表示一个化学反应的( )
| A. | Fe+Cu2+═Fe2++Cu | |
| B. | Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | Cl2+H2O═H++Cl-+HClO | |
| D. | CO32-+2H+═CO2↑+H2O |
16.欧盟定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫.请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)焦炭可用于制取水煤气.测得12g 碳与水蒸气完全反应生成水煤气时,吸收了131.6
kJ热量.该反应的热化学方程式:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.6kJ•mol-1 .
(2)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
①写出NO与活性炭反应的化学方程式C(s)+2NO(g)?N2(g)+CO2(g).
②上述反应T1℃时的平衡常数为 K1,T2℃时的平衡常数为 K2.
Ⅰ.K1=0.5625.(列式并计算)
Ⅱ.根据上述信息判断,温度T1和T2的关系是(填序号)c.
a.T1>T2 b.T1<T2 c.无法比较
(3)CO2经常用氢氧化钠溶液来吸收,现有0.4molCO2,若用200mL 3mol/L NaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有很高的发电效率,因而受到重视,该电池用 Li2CO3 和 Na2CO3 的熔融盐混合物作电解质,CO 为负极燃气,空气与 CO2 的混合气为正极助燃气,制得在 650℃下工作的燃料电池,其负极反应式:2CO-4e-+2CO32-═4CO2,则正极反应式为:O2+2CO2+4e-=2CO32-.
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mo1/L,则生成沉淀所需CaCl2溶液的最小浓度为5.6×10-5mo1/L.
(1)焦炭可用于制取水煤气.测得12g 碳与水蒸气完全反应生成水煤气时,吸收了131.6
kJ热量.该反应的热化学方程式:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.6kJ•mol-1 .
(2)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
 | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②上述反应T1℃时的平衡常数为 K1,T2℃时的平衡常数为 K2.
Ⅰ.K1=0.5625.(列式并计算)
Ⅱ.根据上述信息判断,温度T1和T2的关系是(填序号)c.
a.T1>T2 b.T1<T2 c.无法比较
(3)CO2经常用氢氧化钠溶液来吸收,现有0.4molCO2,若用200mL 3mol/L NaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有很高的发电效率,因而受到重视,该电池用 Li2CO3 和 Na2CO3 的熔融盐混合物作电解质,CO 为负极燃气,空气与 CO2 的混合气为正极助燃气,制得在 650℃下工作的燃料电池,其负极反应式:2CO-4e-+2CO32-═4CO2,则正极反应式为:O2+2CO2+4e-=2CO32-.
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mo1/L,则生成沉淀所需CaCl2溶液的最小浓度为5.6×10-5mo1/L.
3.毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2•2H2O的流程如图:

(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快;直接蒸干BaCl2溶液能(填“能”或“不能”)得到BaCl2•2H2O晶体.
(2)
加入NH3•H2O调节pH=8可除去Fe3+(填离子符号),滤渣Ⅱ中含Mg(OH)2、Ca(OH)2(填化学式).加入H2C2O4时应避免过量,原因是H2C2O4过量会导致生成BaC2O4沉淀,产品的产量减少.
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9.
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42-+2H+═Cr2O72-+H2O Ba2++CrO42-═BaCrO4↓
步骤Ⅰ移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL.
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.BaCl2溶液的浓度为$\frac{b(V0-V1)}{y}$mol•L-1.

(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快;直接蒸干BaCl2溶液能(填“能”或“不能”)得到BaCl2•2H2O晶体.
(2)
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9.
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42-+2H+═Cr2O72-+H2O Ba2++CrO42-═BaCrO4↓
步骤Ⅰ移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL.
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.BaCl2溶液的浓度为$\frac{b(V0-V1)}{y}$mol•L-1.
20.下列反应的离子方程式中错误的是( )
| A. | 氯化铝溶液中加入过量的氨水Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 用醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 将铁屑加入Cu2+溶液中:Fe+Cu2+═Fe2++Cu | |
| D. | 将铝片放入过量NaOH溶液中2Al+2OH-+2H2O═2AlO2-+3H2↑ |
1.下列离子方程式书写正确的是( )
| A. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 硝酸钾溶液与稀硫酸反应:NO3-+H+═HNO3 | |
| C. | 铁与硫酸铜溶液反应:2Fe+3Cu2+═2Fe3++3Cu | |
| D. | 碳酸钠溶液与稀硫酸反应:2H++CO32-═H2O+CO2↑ |
 .
.