题目内容
在下列溶液中,各组离子一定能够大量共存的是( )
| A、滴入甲基橙试液显红色的溶液:Mg2+、Al3+、Br-、SO42- |
| B、常温下,c(H+)/c(OH-)=1010的溶液中:Na+、NH4+、ClO-、I- |
| C、0.1mol/LNaHCO3溶液中:K+、Ba2+、OH-、Cl- |
| D、水电离出的c(H+)=10-12mol/L中:Ba2+、K+、Cl-、CO32- |
考点:离子共存问题
专题:离子反应专题
分析:A.滴入甲基橙试液显红色的溶液呈酸性;
B.常温下,c(H+)/c(OH-)=1010的溶液呈酸性;
C.碱性条件下HCO3-不能大量共存;
D.水电离出的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性.
B.常温下,c(H+)/c(OH-)=1010的溶液呈酸性;
C.碱性条件下HCO3-不能大量共存;
D.水电离出的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性.
解答:
解:A.滴入甲基橙试液显红色的溶液呈酸性,酸性条件下,离子之间不发生任何反应,可大量共存,故A正确;
B.常温下,c(H+)/c(OH-)=1010的溶液呈酸性,酸性条件下,ClO-、I-发生氧化还原反应,不能大量共存,故B错误;
C.碱性条件下HCO3-不能大量共存,故C错误;
D.Ba2+、CO32-反应生成沉淀而不能大量共存,故D错误.
故选A.
B.常温下,c(H+)/c(OH-)=1010的溶液呈酸性,酸性条件下,ClO-、I-发生氧化还原反应,不能大量共存,故B错误;
C.碱性条件下HCO3-不能大量共存,故C错误;
D.Ba2+、CO32-反应生成沉淀而不能大量共存,故D错误.
故选A.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的考查,注意把握常见离子的性质,题目难度不大.

练习册系列答案
相关题目
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法正确的是( )
| A、X、M的原子能形成两种阴阳离子数目之比都为1:2的离子化合物 |
| B、由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
| C、元素Y、Z、W的单质晶体属于同种类型的晶体 |
| D、元素W和M均有多种单质 |
在恒温、恒容的条件下,有反应2A(g)+2B(g)?C(g)+3D(g),现从两条途径分别建立平衡.途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L.则以下叙述正确的是( )
A、达平衡时,途径Ⅰ所得混合气的密度为途径Ⅱ所得混合气密度的
| ||
| B、两途径最终达到平衡时,体系内混合气的百分组成相同 | ||
| C、达平衡时,途径Ⅰ的反应速率v(A)等于途径Ⅱ的反应速率v(A) | ||
| D、两途径最终达到平衡时,体系内混合气的百分组成不同 |
保健医生提示:胃酸过多的人,不宜多吃苹果,因为苹果汁的pH( )
| A、大于7 | B、等于7 |
| C、小于7 | D、不确定 |
 为了测定某NaOH样品中NaOH的质量分数(杂质不参与反应),某化学兴趣小组进行了如下实验:
为了测定某NaOH样品中NaOH的质量分数(杂质不参与反应),某化学兴趣小组进行了如下实验: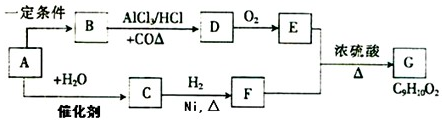
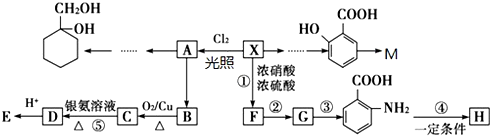
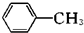
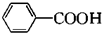
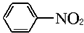
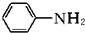 (苯胺,易被氧化)
(苯胺,易被氧化)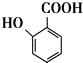 生成高分子化合物M的化学方程式:
生成高分子化合物M的化学方程式: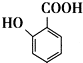 有多种同分异构体,其中含有1个醛基和1个羟基的芳香族化合物有
有多种同分异构体,其中含有1个醛基和1个羟基的芳香族化合物有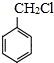 和其他无机化合物合成
和其他无机化合物合成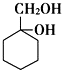 最合理步骤的反应类型依次是:
最合理步骤的反应类型依次是: