题目内容
下列离子方程式正确的是( )
| A、铁和盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、足量碳酸氢钠溶液中滴加少量的石灰水:2HCO3-+Ca2++2 OH-═CaCO3↓+CO32-+2H2O |
| C、碳酸钙溶于稀醋酸:CO32-+2H+=H2O+CO2↑ |
| D、氯化钙溶液与CO2的反应:CO2+Ca2++H2O═CaCO3↓+2H+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.盐酸具有弱氧化性,能铁氧化为亚铁离子;
B.二者反应生成碳酸钙、碳酸钠和水;
C.碳酸钙难溶于水,写化学式;
D.碳酸酸性小于盐酸,所以碳酸和氯化钙不反应.
B.二者反应生成碳酸钙、碳酸钠和水;
C.碳酸钙难溶于水,写化学式;
D.碳酸酸性小于盐酸,所以碳酸和氯化钙不反应.
解答:
解:A.盐酸具有弱氧化性,能铁氧化为亚铁离子,离子方程式为Fe+2H+═Fe2++H2↑,故A错误;
B.二者反应生成碳酸钙、碳酸钠和水,离子方程式为2HCO3-+Ca2++2 OH-═CaCO3↓+CO32-+2H2O,故B正确;
C.碳酸钙难溶于水,写化学式,离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,故C错误;
D.碳酸酸性小于盐酸,所以碳酸和氯化钙不反应,所以没有离子方程式,故D错误;
故选B.
B.二者反应生成碳酸钙、碳酸钠和水,离子方程式为2HCO3-+Ca2++2 OH-═CaCO3↓+CO32-+2H2O,故B正确;
C.碳酸钙难溶于水,写化学式,离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,故C错误;
D.碳酸酸性小于盐酸,所以碳酸和氯化钙不反应,所以没有离子方程式,故D错误;
故选B.
点评:本题考查离子方程式的书写,为高考高频点,明确物质的性质及离子方程式书写规则是解本题关键,注意要遵循客观事实、原子守恒、电荷守恒及转移电子守恒,易错选项是A,注意硝酸能将少量铁氧化为铁离子.

练习册系列答案
相关题目
下列物质转化关系中,需要加入适当氧化剂的是( )
| A、PCl3→PCl5 |
| B、MnO4-→Mn2+ |
| C、SO3→SO42- |
| D、CO2→CO |
物质分类是化学研究的重要方法之一,下列物质分类的正确组合是( )
| 混合物 | 碱 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | 液氧 | 苛性钠 | 胆矾[ | 氧化铁 | 二氧化碳 |
| B | 盐酸 | 烧碱 | 食盐 | 氧化钠 | 一氧化碳 |
| C | 碘酒 | 纯碱 | 石灰石 | 氨气 | 水 |
| D | 大理石 | 熟石灰 | 纯碱 | 生石灰 | 二氧化硫 |
| A、A | B、B | C、C | D、D |
在氯水中存在多种分子和离子,他们在不同的反应中表现出各自的性质.下列实验现象和结论不一致的是( )
| A、加入有色布条,一会儿布条退色,说明溶液中有HClO存在 |
| B、溶液呈黄绿色,且有刺激性气味,说明有Cl2分子存在 |
| C、加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在 |
| D、加入Na2CO3溶液,有气体生成,说明HClO存在 |
在下列溶液中,各组离子一定能够大量共存的是( )
| A、在含有NaHCO3的溶液中:K+、SO42-、Cl-、Al3+ |
| B、使甲基橙变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、水电离的c(H+)=10-11 mol?L-1的溶液:NH4+、K+、ClO-、Cl- |
能正确表示下列化学反应的离子方程式的是( )
| A、氢氧化钡溶液与盐酸的反应 2OH-+2H+=2H2O |
| B、澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O |
| C、铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag |
| D、碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
下列关于金属的描述不正确的是( )
| A、地壳中含量最多的金属元素是Al |
| B、金属一般是热和电的良导体 |
| C、自然界中绝大多数金属元素以游离态的形式存在 |
| D、金属一般呈银白色具有金属光泽 |
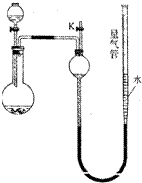 某同学设计如图所示装置(夹持装置已略去,量气管可上下移动)可分别进行下列实验探究
某同学设计如图所示装置(夹持装置已略去,量气管可上下移动)可分别进行下列实验探究