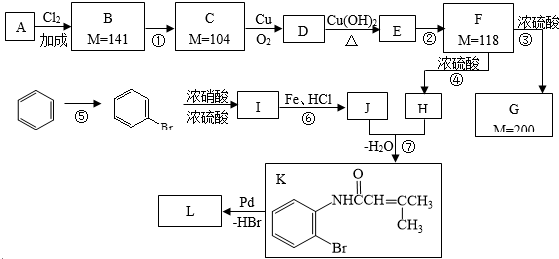
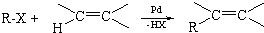题目内容
下列除去杂质的方法不正确的是( )
| A、镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| B、用过量氨水除去Fe3+溶液中的少量Al3+ |
| C、Al(OH)3中混有少量Mg(OH)2:加入过量烧碱溶液充分反应,过滤,向滤液中通入过量CO2后过滤 |
| D、可以用过量氢氧化钠溶液除去MgO中的少量Al2O3 |
考点:物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.铝可与氢氧化钠溶液反应;
B.Fe3+和Al3+都可与氨水反应生成沉淀;
C.氢氧化铝为两性氢氧化物,可与氢氧化钠溶液反应;
D.氧化铝为两性氧化物,可与氢氧化钠反应.
B.Fe3+和Al3+都可与氨水反应生成沉淀;
C.氢氧化铝为两性氢氧化物,可与氢氧化钠溶液反应;
D.氧化铝为两性氧化物,可与氢氧化钠反应.
解答:
解:A.镁和氢氧化钠不反应,而铝可与氢氧化钠溶液反应,可用于除杂,故A正确;
B.Fe3+和Al3+都可与氨水反应生成沉淀,应先加入过量氢氧化钠溶液,过滤后再加入盐酸,故B错误;
C.氢氧化铝为两性氢氧化物,可与氢氧化钠溶液反应,反应后溶液再通入二氧化碳气体可又生成氢氧化铝,可用于除杂,故C正确;
D.氧化铝为两性氧化物,可与氢氧化钠反应,可用于除杂,故D正确.
故选B.
B.Fe3+和Al3+都可与氨水反应生成沉淀,应先加入过量氢氧化钠溶液,过滤后再加入盐酸,故B错误;
C.氢氧化铝为两性氢氧化物,可与氢氧化钠溶液反应,反应后溶液再通入二氧化碳气体可又生成氢氧化铝,可用于除杂,故C正确;
D.氧化铝为两性氧化物,可与氢氧化钠反应,可用于除杂,故D正确.
故选B.
点评:本题考查物质的分离提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,本题着重于铝及其化合物的性质的考查,难度不大,注意把握物质的性质的异同.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、Fe(OH)3、FeCl2均可由化合反应制得 |
| B、配制1L0.1mol/LNa2CO3溶液,需称取Na2CO3?H2O的质量为10.6g |
| C、用澄清石灰水可鉴别CO2和SO2 |
| D、用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
25℃时,下列各组溶液混合后,溶液一定呈中性的是( )
| A、等体积、等物质的量浓度的氨水与盐酸混合 |
| B、pH之和为14的氨水与硝酸等体积混合 |
| C、pH之和为14的Ba(OH)2溶液与NaHSO4溶液等体积混合 |
| D、等体积、等物质的量浓度的Ca(OH)2溶液与Na2CO3溶液混合 |
下列与实验相关的叙述中,正确的是( )
| A、加热NH4C1晶体时,将湿润的红色石蕊试纸靠近试管口,检验NH3的生成 |
| B、向某溶液中加入足量盐酸酸化,无现象,再加入BaCl2溶液,有白色沉淀生成,说明原溶液中存在SO42- |
| C、取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| D、用饱和碳酸钠溶液除去二氧化碳中的氯化氢 |
用石灰水、小苏打、淀粉和食醋等不能完成的实验是( )
| A、鸡蛋壳主要成分的检验 |
| B、食盐和纯碱的鉴别 |
| C、碘盐中碘的检验 |
| D、暖瓶中水垢的除去 |
下列关于工业生产的说法中,不正确的是( )
| A、工业上,用焦炭在电炉中还原二氧化硅得到含少量杂质的粗硅 |
| B、在高炉炼铁的反应中,焦炭为铁矿石的还原剂 |
| C、工业上将粗铜进行精炼,应将粗铜连接电源的正极 |
| D、生产普通玻璃的主要原料有石灰石、石英和纯碱 |
下列操作,能使水的电离平衡向右移动,且使所得溶液显酸性的是( )
| A、在水中加入少量氯化钠,并加热到100℃ |
| B、在水中滴人稀硫酸 |
| C、在水中加入小苏打 |
| D、在水中加入氯化铝固体 |
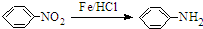 .请回答下列问题:
.请回答下列问题: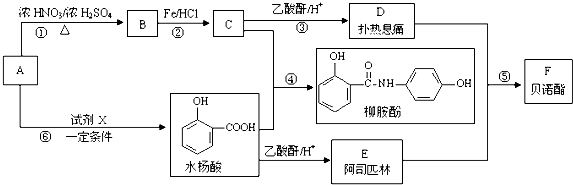
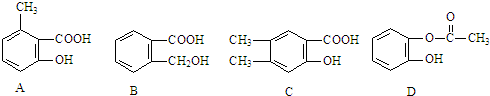
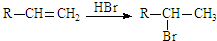 (主产物)
(主产物)