题目内容
9.下列化学反应速率,前者一定大于后者的是( )| A. | G+H=W,其它条件相同时,分别在200℃和100℃下进行反应 | |
| B. | 相同温度下,颗粒相同的锌粒分别与H+浓度相同的硫酸和盐酸反应 | |
| C. | A+B=C(500℃下进行) D+E=F(100℃下进行) | |
| D. | 相同温度下,锌粒与铁粉分别与同浓度的盐酸反应 |
分析 影响化学反应速率的主要因素为物质的本身性质,为内因,对于同一个化学反应来说,增大浓度、压强,升高温度或加入催化剂、增大固体表面积等,可增大反应速率,以此解答该题.
解答 解:A.对于同一个化学反应,升高温度,反应速率增大,故A正确;
B.相同温度下,颗粒相同的锌粒分别与H+浓度相同的硫酸和盐酸反应,氯离子的反应有催化作用,反应较快,故B错误;
C.反应不同,不能确定反应速率大小,故C错误;
D.锌比铁活泼,反应速率较大,故D正确.
故选D.
点评 本题考查化学反应速率,为高频考点,侧重于学生的分析能力的考查,注意把握影响化学反应速率的因素,易错点为C,难度不大.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案
相关题目
19.下列物质中属于弱电解质的是( )
| A. | CO2 | B. | NH3•H2O | C. | NH4NO3 | D. | 酒精 |
20.广告称某品牌的八宝粥(含桂圆、红豆、糯米0不加糖,比加糖还甜,适合糖尿病人食用.你认为下列判断不正确的是( )
| A. | 这个广告有误导喜爱甜食消费者的嫌疑 | |
| B. | 糖尿病人应少吃含糖的食品,该八宝粥未加糖,可以放心食用 | |
| C. | 不加糖不等于没有糖,糖尿病人食用需慎重 | |
| D. | 不能听从厂商或广告商的宣传,应询问医生 |
4.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 17gOH-中所含电子数为10NA | |
| B. | Na2O2固体中的阳离子和阴离子个数比是1:1 | |
| C. | 9g重水(${\;}_{1}^{2}$D2O)所含有的电子数为5NA | |
| D. | 在标准状况下,11.2L氖气含有NA个氖原子 |
14.海水是巨大的资源宝库,海水中主要离子的含量如表所示.
从海水中提取食盐和溴的工艺流程如图:
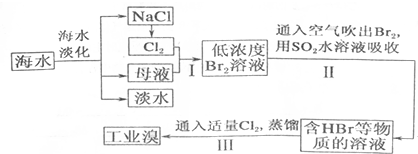
(1)请列举海水淡化的一种方法蒸留法或电渗透法或离子交换法等.
(2)请写出步骤I反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
(3)步骤I中已经获得Br2,步骤II中又将获得的Br2还原为Br-,其目的是富集溴元素.
(4)步骤II用SO2水溶液吸收Br2,吸收率可达95%,该反应的离子方程式为SO2+Br2+2H2O═4H++2Br-+SO42-.
(5)依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为179.2L(忽略Cl2的溶解)
| 成分 | 含量(mg•L-1) | 成分 | 含量(mg•L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Br- | 64 |
| Mg2+ | 1272 |

(1)请列举海水淡化的一种方法蒸留法或电渗透法或离子交换法等.
(2)请写出步骤I反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
(3)步骤I中已经获得Br2,步骤II中又将获得的Br2还原为Br-,其目的是富集溴元素.
(4)步骤II用SO2水溶液吸收Br2,吸收率可达95%,该反应的离子方程式为SO2+Br2+2H2O═4H++2Br-+SO42-.
(5)依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为179.2L(忽略Cl2的溶解)
18.下列化合物中,含有离子键的是( )
| A. | CO2 | B. | HCl | C. | NH3 | D. | NaCl |
9.用惰性电极电解下列各溶液,经一段时间后,溶液的浓度增大,而溶液pH值保持不变的是( )
| A. | CuCl2溶液 | B. | KCl溶液 | C. | H2SO4溶液 | D. | K2SO4溶液 |
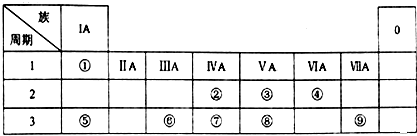
 .
. ⑧的最高价氧化物的水化物的分子式H3PO4.
⑧的最高价氧化物的水化物的分子式H3PO4. .
.