题目内容
5.下列说法不正确的是( )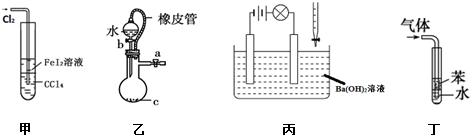
| A. | 甲装置可以用于比较Fe3+、I2、Cl2的氧化性强弱 | |
| B. | 乙装置中打开分液漏斗活塞,水不能顺利流下,说明该装置气密性良好 | |
| C. | 丙装置中若向Ba(OH)2溶液中逐滴加入硫酸溶液直至过量,灯光会由亮变暗至熄灭后又逐渐变亮 | |
| D. | 丁装置不能用于吸收HCl气体及防倒吸 |
分析 A.氯气将亚铁离子氧化生成铁离子,而使水层呈黄色;氯气氧化碘离子生成碘单质,碘单质易溶于四氯化碳而使液体呈紫色;
B.橡胶管上下连通;
C.溶液的导电性强弱与离子的浓度成正比,离子浓度越大导电性越强;
D.有缓冲装置的能防倒吸.
解答 解:A.氯气将亚铁离子氧化生成铁离子,而使水层呈黄色;氯气氧化碘离子生成碘单质,碘单质易溶于四氯化碳而使液体呈紫色,根据哪层液体先变色来判断氧化性强弱,故A正确;
B.橡胶管上下连通,无法检验气密性,故B错误;
C.丙装置中若向Ba(OH)2溶液中逐滴加入硫酸溶液直至过量,硫酸和氢氧化钡反应生成硫酸钡和水,离子浓度减小,溶液导电性减弱,当二者恰好完全反应时溶液中没有溶质,导电性最弱,继续加入稀硫酸,溶液中离子浓度增大,导电性增强,故C正确;
D.水密度大于苯,HCl极易溶于水,该装置没有缓冲作用,不能防止倒吸,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及氧化性比较、试验基本操作、气体收集等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大,易错选项是C.

练习册系列答案
相关题目
16.下列各组中两个变化所发生的反应,属于同一类型的是( )
①由乙烯、氢气制取乙烷、由乙烷、溴(气体)制溴乙烷
②乙烯使溴水褪色、乙炔使酸性高锰酸钾水溶液褪色
③由乙醇、乙酸制乙酸乙酯、由甘氨酸制得二肽
④由乙烯、氯化氢制取氯乙烷、由乙炔、氯化氢制取氯乙烯.
①由乙烯、氢气制取乙烷、由乙烷、溴(气体)制溴乙烷
②乙烯使溴水褪色、乙炔使酸性高锰酸钾水溶液褪色
③由乙醇、乙酸制乙酸乙酯、由甘氨酸制得二肽
④由乙烯、氯化氢制取氯乙烷、由乙炔、氯化氢制取氯乙烯.
| A. | 只有②③ | B. | 只有③④ | C. | 只有①③ | D. | 只有①④ |
13.下列叙述错误的是( )
| A. | 氢氧燃料电池是一种将化学能转化为电能的装置 | |
| B. | 铁船舶的外壳上镶嵌锌块,可避免船体遭受腐蚀 | |
| C. | 钢铁腐蚀时负极的电极反应式:Fe-3e-═Fe+ | |
| D. | 工业上电解饱和食盐水时阴极的电极反应式:2H++2e-═H2↑ |
10.下表是某矿泉水的部分标签说明

则该饮用水中还可能较大量存在的离子是( )

则该饮用水中还可能较大量存在的离子是( )
| A. | OH- | B. | Ag+ | C. | Na+ | D. | Ba2+ |
17.有关Na2CO3和NaHCO3的叙述中正确的是( )
| A. | Na2CO3溶液和NaHCO3溶液可用澄清石灰水鉴别 | |
| B. | NaHCO3比Na2CO3热稳定性强 | |
| C. | 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同 | |
| D. | 在饱和的碳酸钠溶液中通入二氧化碳溶液变浑浊 |
14.我国古代四大发明之一的黑火药爆炸时的反应为:S+2KNO3+3C═K2S+N2↑+3CO2↑,下列关于该反应的说法正确的是( )
| A. | 氧化剂只有KNO3 | B. | C发生还原反应 | C. | KNO3被氧化 | D. | S得到了电子 |
15.40℃时,在氨一水体系中不断通入C02,各种离子的变化趋势如图所示:
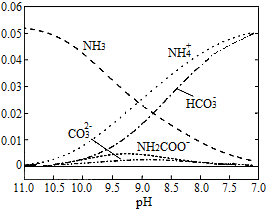 ,
,
下列说法不正确的是( )
 ,
,下列说法不正确的是( )
| A. | 在pH=8.0 时,c(NH4+)>c(HCO3-)>c(NH2COO-)=c(CO32-) | |
| B. | 随着C02的不断通入,Kw不变,但是水的电离受到促进 | |
| C. | 在溶液中pH不断降低的过程中,最终产物中含有NH2COO- | |
| D. | D、随着C02的通入,$\frac{c(O{H}^{-})}{c(N{H}_{3}{H}_{2}O)}$ 不断减小 |
 合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用.
合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用.