题目内容
如图,隔板K可左右移动,甲中充入2 mol A和1
mol B,乙中充入2 mol C和1 mol He,此时K停在0处。发生反应2A(g)+B(g)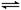 2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是
2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是
A.达平衡后,隔板K最终停留在左侧刻度0~2之间
B.若平衡时K停留在左侧1处,则活塞停留在右侧6处
C.达到平衡时,甲容器中B的物质的量小于于乙容器中B的物质的量
D.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
B
【解析】反应是体积减小的可逆反应,所以在反应过程中乙中气体的物质的量增加,甲中气体的物质的量减少,因此K向作移动。由于是可逆反应,所以甲中气体的物质的量一定大于2mol,因此隔板K最终停留在左侧刻度0~2之间,A正确。乙容器相当于在甲容器的基础上,平衡时通入稀有气体,在压强不变的情况下,平衡向生成A、B的方向移动,所以选项C正确。当K不再滑动时,说明反应达到平衡状态,D正确。若平衡时K停留在左侧1处,则乙中气体的物质的量变化量大于1个单位,所以B不正确,答案选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)
|

A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
B.达到平衡后,隔板K最终停留在左侧刻度0~2之间
C.到达平衡时,甲容器中C的物质的量大于乙容器中C的物质的量
D.若平衡时K停留在左侧1处,则活塞仍停留在右侧6处
如图,隔板K可左右移动,甲中充入2 mol A和1 mol B,乙中充入2 mol C和1 mol He,此时K停在0处。发生反应2A(g)+B(g)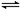 2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是
2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是
| A.达平衡后,隔板K最终停留在左侧刻度0~2之间 |
| B.若平衡时K停留在左侧1处,则活塞停留在右侧6处 |
| C.达到平衡时,甲容器中B的物质的量小于于乙容器中B的物质的量 |
| D.根据隔板K滑动与否可判断左右两边的反应是否达到平衡 |
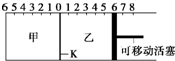 如图,隔板K可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.发生反应2A(g)+B(g)?2C(g),达到平衡后,恢复至温度.下列有关说法不正确 的是
如图,隔板K可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.发生反应2A(g)+B(g)?2C(g),达到平衡后,恢复至温度.下列有关说法不正确 的是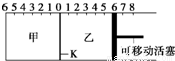 如图,隔板K可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.发生反应2A(g)+B(g)?2C(g),达到平衡后,恢复至温度.下列有关说法不正确 的是
如图,隔板K可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.发生反应2A(g)+B(g)?2C(g),达到平衡后,恢复至温度.下列有关说法不正确 的是