题目内容
多种氧化剂和多种还原剂共存时,存在“争先恐后,强者优先”现象.请理论预测,在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出来的是( )
| A、Mg | B、Cu |
| C、Ag | D、H2 |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题,元素及其化合物
分析:根据金属活动性顺序:Mg>Zn>Cu>Ag,把锌粉加入Cu(NO3)2、Mg(NO3)2和AgNO3的混合溶液中,先和AgNO3反应置换出AgNO3中的Ag,然后和Cu(NO3)2发生反应置换出Cu(NO3)2中的Cu,不和溶液中的Mg(NO3)2发生反应.
解答:
解:向Cu(NO3)2、Mg(NO3)2和AgNO3的混合溶液中加入适量的锌粉,锌粉先和氧化性强的离子反应,则先和AgNO3反应置换出AgNO3中的Ag,然后和Cu(NO3)2发生反应置换出Cu(NO3)2中的Cu,不和溶液中的Mg(NO3)2发生反应.所以首先置换出的是Ag.
故选C.
故选C.
点评:本题考查了氧化还原反应,主要考查了金属之间的置换反应,置换的先后顺序为:活动性最弱的金属最先置换出来,然后依活动性由弱到强依次置换,题目难度不大.

练习册系列答案
相关题目
下列有关环境保护的说法不正确的是( )
| A、“白色污染”是废塑料制品造成的环境污染现象 |
| B、生活废水中含氮、磷等元素,过多排放会引起水体污染 |
| C、对煤等燃料进行脱硫处理后,可减少燃烧产物中SO2的含量 |
| D、汽车使用乙醇汽油不会排放有害气体,故不必安装尾气净化装置 |
下列说法正确的是( )
| A、100g质量分数为46%的乙醇溶液中,共有14mol共价键 |
| B、1个苯分子中含有3个碳碳双键 |
| C、乙烯和苯都能使溴水褪色,褪色的原理相同 |
| D、甲苯分子中所有原子都处于同一平面内 |
在化合反应、分解反应、置换反应、复分解反应四种化学反应中,可能有元素化合价发生变化的反应类型有( )
| A、一种 | B、两种 | C、三种 | D、四种 |
膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢.以下关于PH3的叙述不正确的是( )
| A、PH3分子中有未成键的孤电子对 |
| B、PH3是极性分子 |
| C、它的分子构型是三角锥形 |
| D、磷原子采用sp2杂化方式 |
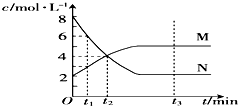 在一定温度下,容器内某一反应中M、N的物质的量浓度随反应时间变化的曲线如图.则下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量浓度随反应时间变化的曲线如图.则下列表述中正确的是( )| A、该反应的化学方程式为2N?M |
| B、t1时,M的浓度是N浓度的2倍 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t2时,正、逆反应速率相等,化学反应达到了平衡 |
固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图Ⅱ表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )


| A、200℃时,反应从开始到平衡的平均速率v(A)=0.08mol?L-1?min-1 |
| B、若0~5min时容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A(g)+B(g)?C(g)△H=+5m kJ/mol |
| C、200℃时,若在第6 min再向体系中充入1mol He,此时v正>v逆 |
| D、200℃时,平衡后再充入2mol C,则达到平衡时,C的体积分数等于0.25 |
下列方法不能用于区分二氧化硫和二氧化碳的是( )
| A、通入品红溶液 |
| B、通入澄清石灰水中 |
| C、通入溴水中 |
| D、通入酸性KMnO4溶液中 |
