题目内容
以下是对某水溶液进行离子检验的方法和结论,其中正确的是
A.先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀。溶液中一定含有大量的SO42-
B.加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定含有大量的CO32-
C.加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体,该气体可以使湿润的红色石蕊试纸变蓝,则溶液中一定含有大量的NH4+
D.先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl-
C
【解析】
试题分析:A.可以和硝酸酸化的氯化钡溶液反应产生的白色沉淀可以是硫酸钡或者是氯化银,所以该澄清溶液中可能含有SO42-或Ag+或SO32-和HSO3-,A错误;B.加入足量的CaCl2溶液,产生了白色沉淀。溶液中可能含有大量的CO32-、SO42-或Ag+或SO32-,B错误;C.加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体,该气体可以使湿润的红色石蕊试纸变蓝,则溶液中一定含有大量的NH4+,C正确;D.先加适量的盐酸将溶液酸化,将溶液中引入了氯离子,再产生白色沉淀,无法说明氯离子的来源,D错误;选C。
考点:考查离子的检验。

练习册系列答案
 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
对下列物质用途的解释不正确的是
用途 | 解释 | |
A | 明矾可用于净水 | 明矾在水中生成的氢氧化铝胶体有吸附性 |
B | SO2可用于漂白纸浆 | SO2具有氧化性 |
C | 小苏打可作糕点的膨松剂 | 受热能分解产生CO2气体 |
D | A1、Fe制容器储存、运输浓硝酸 | 浓硝酸具有强氧化性,遇铁铝发生钝化 |
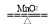 2KCl+3O2↑
2KCl+3O2↑ K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑  2H2↑+O2↑
2H2↑+O2↑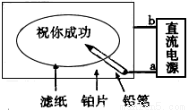
 2NH3 B、H2 (g) + I2 (g)
2NH3 B、H2 (g) + I2 (g)