题目内容
下列有关说法不正确的是( )
| A、镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| B、手机上用的锂离子电池属于二次电池 |
| C、使用催化剂可改变工业合成NH3的反应限度 |
| D、生物质能本质上是太阳能 |
考点:金属的电化学腐蚀与防护,反应热和焓变
专题:化学反应中的能量变化
分析:A.作原电池负极的金属加速被腐蚀,作原电池正极的金属被保护;
B.能多次充放电的电池为二次电池;
C.催化剂只能改变反应速率,不能改变平衡移动;
D.生物质能来源于太阳能.
B.能多次充放电的电池为二次电池;
C.催化剂只能改变反应速率,不能改变平衡移动;
D.生物质能来源于太阳能.
解答:
解:A.Cu、Fe和电解质溶液构成原电池,Fe易失电子作负极、Cu作正极,所以Fe加速被腐蚀,故A正确;
B.锂离子电池能多次充放电,属于二次电池,故B正确;
C.催化剂只能改变反应速率,不能改变平衡移动,所以只能改变反应时间,不能改变反应限度,故C错误;
D.生物质能是太阳能转化而来的,所以生物质能本质上是太阳能,故D正确;
故选C.
B.锂离子电池能多次充放电,属于二次电池,故B正确;
C.催化剂只能改变反应速率,不能改变平衡移动,所以只能改变反应时间,不能改变反应限度,故C错误;
D.生物质能是太阳能转化而来的,所以生物质能本质上是太阳能,故D正确;
故选C.
点评:本题考查基本概念、基本理论,侧重学生对基础知识的掌握,注意催化剂特点,易错选项是C.

练习册系列答案
相关题目
将一定量的NaHCO3和Na2O2的混合物置于一密闭容器中充分加热,反应中转移的电子数为1mol,下列说法一定正确的是( )
| A、混合物中NaHCO3和Na2O2物质的量一定相等 |
| B、容器中肯定有0.5molO2 |
| C、反应后,容器中的固体只有Na2CO3 |
| D、反应后,容器中一定没有H2O |
在酸性溶解中能大量共存的一组离子是( )
| A、Na+、Al3+、Cl-、CO32- |
| B、Na+、Fe2+、SO42-、NO3- |
| C、K+、Ca2+、Cl-、NO3- |
| D、K+、NH4+、OH-、SO42- |
书写热化学方程式要注明物质的聚集状态,原因是( )
| A、具体说明反应的情况 |
| B、说明反应条件 |
| C、物质呈现的状态与反应焓变有关 |
| D、物质呈现的状态与生成什么物质有关 |
下列关于乙醇的说法正确的是( )
| A、用萃取分液的方法除去酒精中的水 |
| B、可由乙烯通过加成反应制取 |
| C、也可用来保存金属钠 |
| D、无水乙醇常用于医疗消毒 |
下列说法正确的是( )
| A、1mol氧气中含有1.204×1024个氧原子,在标准状况下体积约为22.4L |
| B、已知某物质的质量和物质的量,无法确定该物质摩尔质量 |
| C、等体积等物质的量浓度的醋酸(CH3COOH)和盐酸溶液中氢离子数比为1:1 |
| D、若NA表示阿伏加德罗常数,1 molFe作为还原剂失去的电子数一定为2NA |
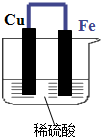 如图示的装置中
如图示的装置中