题目内容
7.下列关于溶液和胶体的叙述正确的是( )| A. | 溶液是电中性的,胶体是带电的 | |
| B. | 胶体粒子可以通过半透膜而溶液不行,故可以用半透膜来分离胶体和溶液 | |
| C. | 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 | |
| D. | 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
分析 A.胶体分散系是电中性的,胶体微粒吸附带电离子;
B.溶液中溶质粒子能通过半透膜;
C.丁达尔现象是胶体的性质,溶液无此现象;
D.溶液中离子运动也是无规律的.
解答 解:A.胶体微粒吸附带电离子,胶体分散系是电中性的,故A错误;
B.溶液中溶质粒子能通过半透膜,胶体中的分散质粒子不能通过,故B错误;
C.一束光线分别通过溶液和胶体时,后者会出现明显光带,前者则没有,故C正确;
D.溶液中溶质微粒不断无规律的运动,故D错误.
故选C.
点评 本题考查了胶体和溶液的区别,胶体性质的应用,难度不大,关键是胶体微粒吸附带电离子的分析判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列离子能大量共存的是( )
| A. | 使无色酚酞试液呈红色的溶液中:Na+、K+、SO42-、CO32- | |
| B. | 无色透明的溶液中:Cu2+、K+、SO42-、NO3- | |
| C. | 含有大量BaCl2的溶液中:Mg2+、NH4+、SO42-、NO3- | |
| D. | 使紫色石蕊试液呈红色的溶液中:Na+、K+、CO32-、NO3- |
18.下列说法不正确的是( )
| A. | 打开盛浓盐酸的试剂瓶可看到白色的酸雾,这说明HCl不稳定 | |
| B. | 蔗糖中滴入浓硫酸,蔗糖变黑,这说明浓硫酸具有脱水性 | |
| C. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| D. | 金属钠存放于煤油中 |
15.用1.000mol/LNaOH溶液滴定0.100mol/LH2SeO3溶液,在下图曲线标注位置,下面什么物质含硒量最少占溶液中硒总量的10%.( )
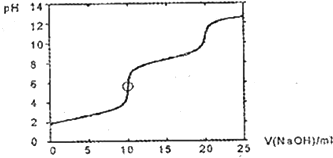

| A. | H2SeO3 | B. | H2SeO3和HSeO3- | C. | HSeO3- | D. | HSeO3-和SeO32- |
2.实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH${\;}_{4}^{+}$+6HCHO═3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1mol H+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ称取样品1.500g.
步骤Ⅱ将样品溶解后,完全转移到250mL容量瓶中,定容、充分摇匀.
步骤Ⅲ移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数偏高(填“偏高”“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积无影响(填“偏大”“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察B.
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由无色变成粉红(或浅红)色.
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.101 0mol•L-1,则该样品中氮的质量分数为18.85%.(保留4位有效数字)
步骤Ⅰ称取样品1.500g.
步骤Ⅱ将样品溶解后,完全转移到250mL容量瓶中,定容、充分摇匀.
步骤Ⅲ移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数偏高(填“偏高”“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积无影响(填“偏大”“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察B.
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由无色变成粉红(或浅红)色.
(2)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
12.下列物质在溶液中电离出的Cl-与1mol CaCl2电离出的Cl-数目相同的是( )
| A. | 2 mol KClO3 | B. | 1 mol KCl | C. | 2 mol MgCl2 | D. | 2 mol NaCl |
16.Na、Cu、O、Si、S、Cl是常见的六种元素.
(1)S的基态原子核外有2个未成对电子;Cu的基态核外电子排布式为1s22s22p63s23p63d104s1.
(2)选填“>”或“<”:
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体.在25℃、101kPa下,已知该反应每消耗1mol CuCl(s),放出热量44.4kJ,该反应的热化学方程式是4CuCl(s)+O2(g)=2CuO(s)+2CuCl2(s)△H=-177.6kJ/mol.
(1)S的基态原子核外有2个未成对电子;Cu的基态核外电子排布式为1s22s22p63s23p63d104s1.
(2)选填“>”或“<”:
| 离子半径 | 酸性 |
| Na+< O2- | H2SO4<HClO4 |
1.下列反应中,不能形成原电池反应的是( )
| A. | 氢氧化钠与盐酸反应 | B. | 金属锌与稀硫酸反应 | ||
| C. | 甲烷燃烧 | D. | 金属铜溶于氯化铁溶液 |