题目内容
9.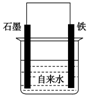 为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是( )
为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是( )| A. | 正极的电极方程式为:O2+2H2O+4e-═4OH- | |
| B. | 将石墨电极改成Mg电极,难以观察到铁锈生成 | |
| C. | 若向自来水中加入少量NaCl(s),可较快地看到铁锈 | |
| D. | 断开连接石墨和铁的导线,铁便不会生锈 |
分析 由吸氧腐蚀原理装置图可知,Fe为负极,石墨为正极,正极上氧气得到电子,向自来水中加入少量NaCl(s),导电性增强,腐蚀速率加快;断开连接石墨和铁的导线,铁发生化学腐蚀,而石墨电极改成Mg电极,Mg作负极,以此来解答.
解答 解:A.钢铁的吸氧腐蚀中,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-═4OH-,故A正确;
B.将石墨换成镁,镁和铁构成的原电池中,镁作负极,容易失去电子被氧化,所以铁被保护,难以观察到铁锈生成,故B正确;
C.向自来水中加入少量氯化钠固体,溶液中自由移动离子增加,腐蚀速率加快,所以可以较快看到铁锈,故C正确;
D.断开连接石墨和铁的导线,铁发生化学腐蚀,铁仍然会生锈,只是腐蚀速率较慢,故D错误;
故选D.
点评 本题考查电化学腐蚀及原电池原理,为高频考点,把握吸氧腐蚀的原理及电极反应为解答的关键,侧重分析与应用能力的考查,注意化学腐蚀的速率小于电化学腐蚀的速率,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
19.下列说法正确的是( )
| A. | 6.02×1023就是阿伏加德罗常数 | |
| B. | 1mol Cl2含有2NA个氯原子 | |
| C. | 摩尔既可表示质量,又可以表示数量 | |
| D. | 32g O2所含O2的摩尔数是1mol |
20.据报道,意大利科学家合成了一种新型的氧分子,它是由四个氧原子构成的.下列关于该分子的叙述正确的是( )
| A. | O4的摩尔质量是64 | B. | O2、O3、O4都是氧的同位素 | ||
| C. | O2、O3、O4都是氧的同素异形体 | D. | O2、O3、O4互为同分异构体 |
17.化学与人类生产、生活、社会可持续发展密切相关.下列有关说法正确的是( )
| A. | 某地燃烧化石燃料排放的废气中含CO2、SO2,使雨水pH=6形成酸雨 | |
| B. | 氟利昂和NOX都能破坏臭氧层,从而导致“温室效应” | |
| C. | 中国是目前全球最大的稀土生产国和出口国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径 | |
| D. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
4.下列反应中属于置换反应的是( )
| A. | 乙醇与金属钠的反应 | B. | 氢氧化铁与稀硫酸的反应 | ||
| C. | 氯化铁溶液与铜片的反应 | D. | 一氧化碳还原氧化铁的反应 |
14.下列物质在氯气中燃烧时,能产生白色烟雾的是( )
| A. | 红磷 | B. | 铜丝 | C. | 氢气 | D. | 金属钠 |
1.在容积固定的密闭容器中发生反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0,容器内部分物质的物质的量浓度如下表:
(1)反应在第2min到第4min时,O2的平均反应速率为0.1875mol•L-1•min-1,a=1.35
(2)反应在第2min到第4min改变了条件,改变的条件可能是加入催化剂.
| 时间/浓度 | C(NH3)(mol•L-1) | C(O2)(mol•L-1) | C(NO)(mol•L-1) |
| 起始 | 0.8000 | 1.600 | 0.000 |
| 第2min | 0.6000 | a | 0.2000 |
| 第4min | 0.3000 | 0.9750 | 0.5000 |
| 第6min | 0.3000 | 0.9750 | 0.5000 |
| 第8min | 0.7000 | 1.475 | 0.1000 |
(2)反应在第2min到第4min改变了条件,改变的条件可能是加入催化剂.
15.常温下,浓度为0.05mol•L-1的H2SO4溶液其PH值为( )
| A. | 2 | B. | 13 | C. | 1 | D. | 1.3 |
