��Ŀ����
��֪2SO2(g)+O2(g)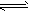 2SO3(g) ��H=��196kJ��mol-1�� 500��ʱ��2mol SO2��1molO2װ��һ����㶨��
2SO3(g) ��H=��196kJ��mol-1�� 500��ʱ��2mol SO2��1molO2װ��һ����㶨��
10L�ܱ������У�2���ӣ�t1��ʱ�ﵽƽ�⡣����ͼ��ʾ��
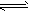 2SO3(g) ��H=��196kJ��mol-1�� 500��ʱ��2mol SO2��1molO2װ��һ����㶨��
2SO3(g) ��H=��196kJ��mol-1�� 500��ʱ��2mol SO2��1molO2װ��һ����㶨��10L�ܱ������У�2���ӣ�t1��ʱ�ﵽƽ�⡣����ͼ��ʾ��
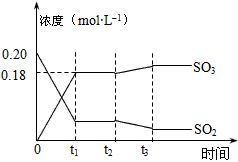
��ش���������
��1����O2��ʾ2�����ڸ÷�Ӧ��ƽ����Ӧ����Ϊ________mol��L-1��min-1������500��ʱ�÷�Ӧ��ƽ�ⳣ��
K=________��
��2����ͼ��ʾ�÷�Ӧ��ʱ��t1�ﵽƽ�����ƽ��ʱO2��ת����________��ʱ��t2��ı�ij�������������仯�������ͼ��ʱ��t2�����ı������������________________��дһ�����ɣ���
��3����������������ʼװ���SO2��O2��2mol����ƽ�����SO3��ת����Ϊx���г���x�ķ���
________________�����������x��
��4��ij�¶�ʱ���÷�Ӧ��ƽ�ⳣ��K=800������¶�________500�棨�������������������������
��1����O2��ʾ2�����ڸ÷�Ӧ��ƽ����Ӧ����Ϊ________mol��L-1��min-1������500��ʱ�÷�Ӧ��ƽ�ⳣ��
K=________��
��2����ͼ��ʾ�÷�Ӧ��ʱ��t1�ﵽƽ�����ƽ��ʱO2��ת����________��ʱ��t2��ı�ij�������������仯�������ͼ��ʱ��t2�����ı������������________________��дһ�����ɣ���
��3����������������ʼװ���SO2��O2��2mol����ƽ�����SO3��ת����Ϊx���г���x�ķ���
________________�����������x��
��4��ij�¶�ʱ���÷�Ӧ��ƽ�ⳣ��K=800������¶�________500�棨�������������������������
��1��0.045��8100
��2��90%������O2Ũ�ȣ����£�
��3��10x2/[(1-x)2(2-x)]=8100
��4����
��2��90%������O2Ũ�ȣ����£�
��3��10x2/[(1-x)2(2-x)]=8100
��4����

��ϰ��ϵ�д�
�����Ŀ
���������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ���ǣ� ��
A����֪2SO2(g)+O2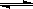 2SO3(g) Ϊ���ȷ�Ӧ����SO2������һ������SO3������ 2SO3(g) Ϊ���ȷ�Ӧ����SO2������һ������SO3������ |
| B����֪C(ʯī,s) ===C�����ʯ,s�� ��H��0������ʯ��ʯī�ȶ� |
| C��NaOH(aq)��HCl(aq)===NaCl(aq)��H2O(l)����H����57.4 kJ/mol����20 g NaOH����Һ������ϡ������ȫ��Ӧ���ų�������Ϊ28.7 kJ |
| D����֪2C(s) +2O2 (g) ===2CO2(g) ��H1 |
 2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����ش��������⣺
2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����ش��������⣺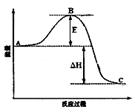
 2SO3(g)(����Ӧ����)������500��ʹ����������£��÷�Ӧ���ݻ��̶����ܱ������н��У������й�˵����ȷ����
2SO3(g)(����Ӧ����)������500��ʹ����������£��÷�Ӧ���ݻ��̶����ܱ������н��У������й�˵����ȷ����