题目内容
①某元素原子的价电子构型为3s23p3,它属于第 周期,是 族,有 个电子层, 个能级, 个价电子, 个未成对电子.最高正化合价为 ,元素名称是 .
②第四周期第六个元素的价电子构型是 ,它是 族, 区元素,元素符号是 .
③按原子序数从锂到氟,第一电离能由小到大的次序是 .
④某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,其核外电子排布式为 ,价电子排布式为 ,属 区元素.
②第四周期第六个元素的价电子构型是
③按原子序数从锂到氟,第一电离能由小到大的次序是
④某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,其核外电子排布式为
考点:元素周期表的结构及其应用,原子核外电子排布,元素电离能、电负性的含义及应用
专题:原子组成与结构专题,元素周期律与元素周期表专题
分析:①由价电子构型为3s23p3,有3个电子层,最外层电子数为5,则为P;
②第四周期第六个元素为Cr;
③原子序数从锂到氟,金属性减弱,非金属性增强,则第一电离能增大,但N的最外层电子半满为稳定结构;
④某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,则为第四周期ⅤB的元素V.
②第四周期第六个元素为Cr;
③原子序数从锂到氟,金属性减弱,非金属性增强,则第一电离能增大,但N的最外层电子半满为稳定结构;
④某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,则为第四周期ⅤB的元素V.
解答:
解:①由价电子构型为3s23p3,有3个电子层,最外层电子数为5,为第三周期VA族元素P,由1s、2s、2p、3s、3p共5个能级,3p上3个电子为未成对电子,最高价等于最外层电子数,为+5价,P的名称为磷,故答案为:三;VA;3;5;5;3;+5;磷;
②第四周期第六个元素为Cr,价电子构型是3d54s2,为ⅥB族元素,最后填充d电子,为d区元素,故答案为:3d54s2;ⅥB;d;Cr;
③原子序数从锂到氟,金属性减弱,非金属性增强,则第一电离能增大,但N的最外层电子半满为稳定结构,则第一电离能由小到大的次序是Li、B、Be、C、O、N、F,故答案为:Li、B、Be、C、O、N、F;
④某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,则为第四周期ⅤB的元素V,核外电子排布式为[Ar]3d34s2,价电子排布式为3d34s2,最后填充d电子,为d区元素,故答案为:[Ar]3d34s2;3d34s2;d.
②第四周期第六个元素为Cr,价电子构型是3d54s2,为ⅥB族元素,最后填充d电子,为d区元素,故答案为:3d54s2;ⅥB;d;Cr;
③原子序数从锂到氟,金属性减弱,非金属性增强,则第一电离能增大,但N的最外层电子半满为稳定结构,则第一电离能由小到大的次序是Li、B、Be、C、O、N、F,故答案为:Li、B、Be、C、O、N、F;
④某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,则为第四周期ⅤB的元素V,核外电子排布式为[Ar]3d34s2,价电子排布式为3d34s2,最后填充d电子,为d区元素,故答案为:[Ar]3d34s2;3d34s2;d.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、性质及电子排布为解答的关键,注意元素的推断及电子排布、价电子排布的区别,题目难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
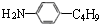 可能有4种异构体,它们是:
可能有4种异构体,它们是: