题目内容
3.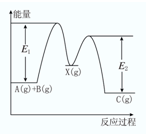 反应A(g)+B(g)→C(g)△H,分两步进行:①A(g)+B(g)→X(g)△H1,②X(g)→C(g)△H2,反应过程中能量变化如图所示,E1表示A(g)+B(g)→X(g)的活化能,下列说法正确的是( )
反应A(g)+B(g)→C(g)△H,分两步进行:①A(g)+B(g)→X(g)△H1,②X(g)→C(g)△H2,反应过程中能量变化如图所示,E1表示A(g)+B(g)→X(g)的活化能,下列说法正确的是( )| A. | △H=E1-E2 | B. | E1是反应①的活化能 | ||
| C. | X是反应A(g)+B(g)→C(g)的催化剂 | D. | △H2>0 |
分析 A.依据盖斯定律来分析△H与E1、E2的关系;
B.分子从常态转变为容易发生化学反应的活跃状态所需要的能量称为活化能;
C.依据催化剂是先作为反应物参与化学反应,然后再通过化学反应转变成原物质;
D.根据反应物与生成物总能量的大小关系判断反应热.
解答 解:A.①A(g)+B(g)→X(g)△H1 ②X(g)→C(g)△H2,①+②得:A(g)+B(g)→C(g)△H=△H1+△H2,故A错误;
B.根据图示可知,E1是气体A、B分子从常态转变为容易发生化学反应的活跃状态所需要的能量,为反应①的活化能,故B正确;
若X是反应A(g)+B(g)→C(g)的催化剂,则X是反应①的反应物,是反应②的生成物,故B错误;
C.若X是反应A(g)+B(g)→C(g)的催化剂,则X是反应①的反应物,是反应②的生成物,则X不是反应A(g)+B(g)→C(g)的催化剂,故C错误;
D.根据图示可知,X(g)的总能量大于C(g),则该反应为放热反应,△H2<0,故D错误;
故选B.
点评 本题考查反应热与焓变的应用,题目难度不大,涉及盖斯定律的应用、化学反应的能量变化与反应的焓变关系的分析判断,反应活化能的判断计算等知识,明确图象曲线变化的含义为解答关键,注意掌握活化能的概念,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
13. 苯乙烯(C8H8)是生产各种塑料的重要单体,其制备原理是:
苯乙烯(C8H8)是生产各种塑料的重要单体,其制备原理是:
C8H10 (g)(乙苯)?C8H8 (g)(苯乙烯)+H2(g),
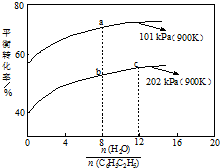
实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),如图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系.下列说法正确的是( )
 苯乙烯(C8H8)是生产各种塑料的重要单体,其制备原理是:
苯乙烯(C8H8)是生产各种塑料的重要单体,其制备原理是:C8H10 (g)(乙苯)?C8H8 (g)(苯乙烯)+H2(g),
实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),如图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系.下列说法正确的是( )
| A. | a点转化率为75%,若起始向1 L恒容容器中充入1 mol 乙苯,则平衡常数为2.25 | |
| B. | b点转化率为50%,则混合气体中苯乙烯的体积分数为$\frac{1}{19}$ | |
| C. | 恒容时加入稀释剂能减小C8H10 (g)平衡转化率 | |
| D. | b点和c点温度和压强相同,所以反应速率也相等 |
14.我国稀土资源丰富,下列有关稀土元素${\;}_{62}^{144}Sm$与${\;}_{62}^{150}Sm$的说法正确的是( )
| A. | ${\;}_{62}^{144}Sm$与${\;}_{62}^{150}Sm$互为同位素 | |
| B. | ${\;}_{62}^{144}Sm$与${\;}_{62}^{150}Sm$的质量数相同 | |
| C. | ${\;}_{62}^{144}Sm$与${\;}_{62}^{150}Sm$是同一种核素 | |
| D. | ${\;}_{62}^{144}Sm$与${\;}_{62}^{150}Sm$的核外电子数和中子数均为62 |
11.下列实验操作中,正确的是( )
| A. | 利用过滤分离溶液和胶体 | |
| B. | 用渗析法可以除去溶液中的胶体粒子 | |
| C. | 向氢氧化钠溶液中边滴加饱和FeCl3溶液边振荡制备Fe(OH)3胶体 | |
| D. | 向Fe(OH)3胶体中加入足量稀盐酸后,依然有丁达尔效应 |
18.关于苯及苯的同系物的说法,不正确的是( )
| A. | 利用甲苯的硝化反应可以制得TNT炸药 | |
| B. | 苯与甲苯互为同系物,可以用KMnO4酸性溶液进行鉴别 | |
| C. | 苯和溴水振荡后,由于发生化学反应而使溴水的水层颜色变浅 | |
| D. | 煤焦油中含有苯和甲苯,用蒸馏的方法把它们分离出来 |
15.大米属于( )
| A. | 中性食品 | B. | 碱性食品 | C. | 弱碱性食品 | D. | 酸性食品 |
12.下列有关Na2CO3和NaHCO3性质的说法中,不正确的是( )
| A. | 热稳定性:Na2CO3>NaHCO3 | |
| B. | 相同温度下,在水中的溶解度Na2CO3>NaHCO3 | |
| C. | 相同质量的Na2CO3和NaHCO3分别与过量盐酸反应,放出CO2质量:Na2CO3>NaHCO3 | |
| D. | Na2CO3 和NaHCO3均可与澄清石灰水反应 |