题目内容
5.现有10种元素的性质、数据如表所列,它们均为短周期元素.| A | B | C | D | E | F | G | H | I | J | |
| 原子半径 (10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | 1.02 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6 | +1 | |
| -2 | -3 | -1 | -3 | -2 |
(1)D的元素名称是磷,若H的一种同位素中子数为5,则其原子符号是${\;}_{5}^{10}$B,B元素的原子结构示意图是
 ;
;(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;化合物F2A2的电子式是:
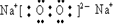 .
.(3)用电子式表示F2I的形成过程:
 ;
;(4)用J元素的单质与A元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的惰性电极甲和乙浸入KOH溶液,在甲极通入J的单质,乙极通入A的单质,则乙极的电极反应式为:O2+4e-+2H2O=4OH-.
分析 由表格在元素的性质可知,+1价的C、F、J,结合原子半径可知,F为Na,C为Li,J为H;A、I均有-2价,且A只有-2价,则A为O,I为S;B最高化合价为+2价,应为第二主族元素,且原子半径F>B>C,则B为Mg元素,D和G最高正价均为+5,负价一致,故为VA族元素,因原子半径D>G,故D为第三周期第VA族的P元素,G为N元素;从化合价可推出E属于卤素,由于短周期F元素无正价,故E为氯元素,位于第VIIA族第三周期;H最高正价+3价,无负价,只能是IIIA族元素,而原子半径H>F,故H只能是位于第二周期第IIIA族的B元素,然后结合元素化合物知识及反应原理来解答.
解答 解:由表格在元素的性质可知,+1价的C、F、J,结合原子半径可知,F为Na,C为Li,J为H;A、I均有-2价,且A只有-2价,则A为O,I为S;B最高化合价为+2价,应为第二主族元素,且原子半径F>B>C,则B为Mg元素,D和G最高正价均为+5,负价一致,故为VA族元素,因原子半径D>G,故D为第三周期第VA族的P元素,G为N元素;从化合价可推出E属于卤素,由于短周期F元素无正价,故E为氯元素,位于第VIIA族第三周期;H最高正价+3价,无负价,只能是IIIA族元素,而原子半径H>F,故H只能是位于第二周期第IIIA族的B元素,
(1)由以上分析可知,D为磷元素,若H的一种同位素中子数为5,则其原子符号是${\;}_{5}^{10}$B,Mg元素的原子结构示意图是 ,
,
故答案为:磷;${\;}_{5}^{10}$B; ;
;
(2)以上元素中,非金属性最强的元素为Cl元素,对应的最高价氧化物的水化物的为HClO4,酸性最强,化合物F2A2为Na2O2,为离子化合物,
故答案为:HClO4;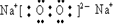 ;
;
(3)用电子式表示Na2S的形成过程为 ,
,
故答案为: ;
;
(4)碱性氢氧燃料电池中,负极发生氧化反应,氢气得电子生成氢氧根离子,电极反应式为H2-2e-+2OH-═2H2O,乙极通入O2的单质,则乙极的电极反应式为O2+4e-+2H2O=4OH-,
故答案为:O2+4e-+2H2O=4OH-.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的化合价、原子半径推断元素为解答的关键,侧重分析与应用能力的考查,注意电子式表示形成过程、原电池原理的应用等为解答的难点,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 与同族硅元素类似,锗、锡、铅都可用做半导体材料 | |
| B. | 锗与盐酸可能不反应,锡、铅能与盐酸反应 | |
| C. | 锗、锡、铅的+4价氢氧化物的碱性由弱到强的顺序为:Ge(OH)4<Sn(OH)4<Pb(OH)4 | |
| D. | 锗、锡、铅的金属性依次减弱 |
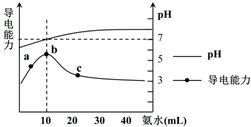
| A. | a~b点导电能力增强说明HR为弱酸 | |
| B. | b点溶液pH=7说明NH4R没有水解 | |
| C. | c 点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) | |
| D. | b-c任意点溶液均有c(H+)•c(OH-)=Kw=1.0×10-14 mol2•L-2 |
| A. | 一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA | |
| B. | 标准状况下,22.4L二氯甲烷的分子数约为NA个 | |
| C. | 含4.8g碳元素的石墨晶体中的共价键数为1.2NA个 | |
| D. | 2mL 0.5mol/L硅酸钠溶液中滴入过量盐酸制备硅酸胶体,所得胶粒数目为0.001NA |
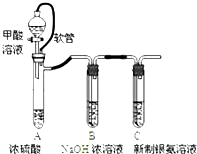 | 已知:①银氨溶液的化学式为: Ag(NH3)2OH ②反应结束后试管C底部有黑色 沉淀生成, ③分离出上层清液和底部黑色 固体备用. |
(2)装置A中软管的作用是平衡漏斗上下压强,使甲酸溶液能顺利滴下.
(3)为验证C中上层清液中产物的成分,进行如下实验:
a.测得上层清液pH为10.
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体.
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象.
①实验c的目的是对比试验,排除银氨溶液对产物检验的干扰.
②根据上述实验现象判断,上层清液中产物成分为(NH4)2CO3(填化学式).
(4)设计实验证明黑色固体的成分是Ag:可供选择的试剂有:浓硫酸、浓硝酸、NaOH溶液、NaCl溶液.取少量上述黑色固体,用蒸馏水洗净,滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl溶液,能产生白色沉淀,说明黑色固体是Ag单质.(补充必要的实验内容及实验现象)
(5)从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2.
①写出生成AgCl沉淀的离子反应[Ag(NH3)2]++OH-+3H++Cl-=AgCl↓+2NH4++H2O.
②若该反应中消耗3.3g羟氨,理论上可得银的质量为10.8g.
 =5SO2-4+2Mn2+ +3H2O
=5SO2-4+2Mn2+ +3H2O
 (R-CH3或-H)
(R-CH3或-H) $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$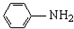
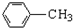 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$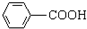
 生成A的反应类型是取代反应.
生成A的反应类型是取代反应.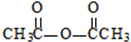 .
. .
.
 .(不用写条件)
.(不用写条件)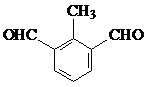 或
或  (任写一种即可).
(任写一种即可).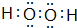 .
.