题目内容
5.研究有机化合物的组成、结构、分类有利于全面认识其性质.①下列有机化合物属于芳香烃的是b(填字母).
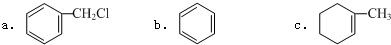
②下列有机化合物不能与NaOH溶液反应的是a(填字母).
a.乙醇 b.苯酚 c.甘氨酸
③下列有机化合物既能发生酯化反应又能发生银镜反应的是c(填字母).
a.HCOOCH2CH3 b.CH3CH2Br c.
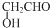
分析 ①芳香烃是含有苯环的CH化合物;
②氢氧化钠与酸和酚反应;
③含有醛基的有机物能发生银镜反应,含有羟基和羧基能发生酯化反应.
解答 解:① ,a中含有-Cl,属于卤代烃,b为苯,属于芳香烃,c中不含有苯环,不是芳香烃,故答案为:b;
,a中含有-Cl,属于卤代烃,b为苯,属于芳香烃,c中不含有苯环,不是芳香烃,故答案为:b;
②乙醇不能与氢氧化钠反应,苯酚为石炭酸,能与氢氧化钠反应,甘氨酸中含有羧基,能与氢氧化钠反应,故答案为:a;
③含有羟基和羧基能发生酯化反应,含有醛基能发生银镜反应,故答案为:c.
点评 本题主要考查的是有机物的分类、有机物的性质等,难度不大.

练习册系列答案
相关题目
15.基因测序研究中,常用${\;}_{15}^{32}$P作标记物,下列关于${\;}_{15}^{32}$P的说法正确的是( )
| A. | 质子数为32 | B. | 质量数为15 | ||
| C. | ${\;}_{15}^{32}$P与${\;}_{15}^{33}$P互为同位素 | D. | 中子数为15 |
13.钢铁淬火时常发生的反应有:2Fe+6H2O$\frac{\underline{\;高温\;}}{\;}$2Fe(OH)3+3H2,该反应属于( )
| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
20. 我国成功研制出新型“海水电池”.电池反应为4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )
我国成功研制出新型“海水电池”.电池反应为4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )
 我国成功研制出新型“海水电池”.电池反应为4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )
我国成功研制出新型“海水电池”.电池反应为4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )| A. | 铝片作负极 | |
| B. | 海水作为电解质溶液 | |
| C. | 电池工作时O2得到电子 | |
| D. | 电池工作时实现了电能向化学能的转化 |
10.一定能在下列溶液中大量共存的离子组是( )
| A. | 碱性溶液:Na+、Ca2+、SO42-、CO32- | |
| B. | 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- | |
| C. | 氯水溶液:H+、Fe2+、SO42-、Cl- | |
| D. | 含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl- |
17.短周期元素A,B,C,D在周期表中的位置如图所示,E2+与D的简单阴离子有相同的电子层结构,D元素原子的次外层电子数等于其他层电子数之和,则下列说法正确的是( )
| A | B | C |
| D |
| A. | C的非金属性最强,可与E元素形成共价化合物 | |
| B. | 元素D可形成三种价态的酸,且酸根离子均能促进水的电离 | |
| C. | 原子半径由大到小的排列顺序为:E>D>B>A>C | |
| D. | C、D元素形成的最简单的氢化物的热稳定性:D<C |
15.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,0.1molC8H18所含有的共价键数目为2.5NA | |
| B. | 1L 1 mol•L-1 FeCl3溶液完全水解产生的Fe(OH)3胶体粒子数为NA | |
| C. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA | |
| D. | 28.6gNa2CO3•10H2O溶于水配成1L溶液,该溶液中阴离子数目为0.1NA |
 煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题:
煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题: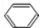 +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O;
+H2O;
 .
.