题目内容
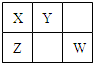 已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图,其中X原子最外层电子数是其电子层数的2倍.下列说法正确的是( )
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图,其中X原子最外层电子数是其电子层数的2倍.下列说法正确的是( )| A、四种元素的原子半径大小rY>rW>rX>rZ |
| B、元素X的含氧酸只有一种,元素Y则有两种 |
| C、元素Z的气态氢化物的稳定性比元素Y的强 |
| D、元素Y和W的氧化物是导致酸雨的主要原因 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W为四种短周期主族元素,根据在周期表中的相对位置,可知X位于第二周期,X原子最外层电子数是其电子层数的2倍,则X为C元素,可推出Y为N元素、Z为Si元素、W为S元素.
A.同周期自左而右原子半径减小,电子层越多原子半径越大;
B.碳元素含氧酸可能为碳酸或羧酸;
C.元素非金属性越强,其氢化物越稳定;
D.S的氧化物和N的氧化物是导致酸雨的主要原因.
A.同周期自左而右原子半径减小,电子层越多原子半径越大;
B.碳元素含氧酸可能为碳酸或羧酸;
C.元素非金属性越强,其氢化物越稳定;
D.S的氧化物和N的氧化物是导致酸雨的主要原因.
解答:
解:X、Y、Z、W为四种短周期主族元素,根据在周期表中的相对位置,X位于第二周期,X原子最外层电子数是其电子层数的2倍,则X为C元素,可推出Y为N元素、Z为Si元素、W为S元素,
A.根据四种元素的相对位置,原子半径大小顺序为:rZ>rW>rX>rY,故A错误;
B.碳元素的含氧酸为羧酸时,有多种,故B错误;
C.根据元素周期律,元素Z的气态氢化物的稳定性比元素Y的弱,故C错误;
D.S的氧化物和N的氧化物是导致酸雨的主要原因,故D正确.
A.根据四种元素的相对位置,原子半径大小顺序为:rZ>rW>rX>rY,故A错误;
B.碳元素的含氧酸为羧酸时,有多种,故B错误;
C.根据元素周期律,元素Z的气态氢化物的稳定性比元素Y的弱,故C错误;
D.S的氧化物和N的氧化物是导致酸雨的主要原因,故D正确.
点评:本题考查元素的推断、元素周期律等,难度不大,注意对元素周期律的理解掌握.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
下列物质结构与对应的用语表达都正确的是( )
| A、S-C-S:二硫化碳的结构式 |
B、 :苯酚的结构简式 :苯酚的结构简式 |
C、 :氯化铵的电子式 :氯化铵的电子式 |
D、 :钠离子的结构示意图 :钠离子的结构示意图 |
用铂电极电解下列溶液时,阴极和阳极上的主要产物分别为H2和O2的是( )
| A、稀NaOH溶液 |
| B、HCl溶液 |
| C、NaCl溶液 |
| D、酸性AgNO3溶液 |
露置的苛性钾经分析含H2O:7.62%,K2CO3:2.38%,KOH:90%,将此样品1g放入1mol?L-1盐酸46mL中,过量的酸用1.070mol?L-1 KOH中和至中性,蒸发中和后的溶液可得固体( )
| A、4.00g | B、3.43g |
| C、4.50g | D、无法计算 |
 五种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
五种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.

 一定条件下,在一个3L密闭容器中发生如图反应:
一定条件下,在一个3L密闭容器中发生如图反应: