题目内容
用NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、常温常压下,48g O2和O3含有的氧原子数均为3NA |
| B、标准状况下,22.4L H2O含有的分子数为NA |
| C、11.2L Cl2中含有的原子数为NA |
| D、2.7g铝与足量氢氧化钠溶液反应转移的电子数NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氧气和臭氧中只含有氧元素,48g氧气和臭氧中含有48g氧原子,含有3mol氧原子;
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氯气的物质的量;
D.铝为3价金属,2.7g铝的物质的量为0.1mol,0.1mol铝完全反应失去0.3mol电子.
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
C.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氯气的物质的量;
D.铝为3价金属,2.7g铝的物质的量为0.1mol,0.1mol铝完全反应失去0.3mol电子.
解答:
解:A.48g氧气和48g臭氧中含有48g氧原子,含有氧原子的物质的量为3mol,含有的氧原子数均为3NA,故A正确;
B.标况下,水不是气体,不能使用标况下的气体摩尔体积计算水的物质的量,故B错误;
C.不是标况下,不能使用标况下的气体摩尔体积计算11.2L氯气的物质的量,故C错误;
D.2.7g铝的物质的量为0.1mol,0.1mol铝完全反应失去0.3mol电子,转移的电子数0.3NA,故D错误;
故选A.
B.标况下,水不是气体,不能使用标况下的气体摩尔体积计算水的物质的量,故B错误;
C.不是标况下,不能使用标况下的气体摩尔体积计算11.2L氯气的物质的量,故C错误;
D.2.7g铝的物质的量为0.1mol,0.1mol铝完全反应失去0.3mol电子,转移的电子数0.3NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.

练习册系列答案
相关题目
下列各组有机化合物中,肯定属于同系物的一组是( )
| A、C2H6 与C5H12 |
| B、C3H6 与C4H8 |
| C、甲醇与乙二醇 |
D、 与 与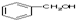 |
防治环境污染,改善生态环境已成为全球的共识.空气质量报告的各项指标能体现空气的质量.下列各项指标不需要监测的是( )
| A、PM--2.5 |
| B、NO2浓度 |
| C、SO2浓度 |
| D、CO2浓度 |
在相同的温度和压强下,二氧化碳和笑气(化学式为N2O)的体积相同,则下列它们的下列物理量中一定相同的是( )
①分子数
②原子数
③密度
④质量
⑤物质的量.
①分子数
②原子数
③密度
④质量
⑤物质的量.
| A、只有①⑤ |
| B、只有①②④⑤ |
| C、只有②③④⑤ |
| D、①②③④⑤ |
下列离子方程式正确的是( )
| A、Zn和浓硫酸反应 Zn+2H+═H2↑+Zn2+ | ||
| B、钠与水反应:Na+2H2O═Na++2OH-+H2↑ | ||
C、硫酸铝溶液与过量氢氧化钠溶液反应:Al3++4OH-═AlO
| ||
D、向Ca(ClO)2溶液中通入少量CO2:ClO-+H2O+CO2═HClO+HCO
|
某学生在配制250ml 0.5mol/L的NaOH溶液时,最终配制的溶液浓度比要求的高,造成该误差的原因可能是( )
| A、称量前天平没调平衡,静止时指针偏向标尺右边 |
| B、配制前容量瓶未干燥 |
| C、定容时仰视 |
| D、洗涤液未全部转移到容量瓶中 |
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A、体积比为8:11 |
| B、密度之比为11:8 |
| C、物质的量之比为11:8 |
| D、原子个数之比为11:12 |
乙炔在不同条件下可以转化成许多化合物,如图,下列叙述错误的是( )


| A、正四面体烷的二氯代物只有1种 |
| B、乙炔生成乙烯基乙炔是加成反应 |
| C、等质量的苯与乙烯基乙炔完全燃烧时的耗氧量不同 |
D、 与环辛四烯互为同分异构体 与环辛四烯互为同分异构体 |