题目内容
10.油条和豆浆是我国传统的早餐食物,炸油条时常用到一种白色物质,它既能中和发酵过程中产生的酸,又能起发泡作用,这种白色物质是( )| A. | NaOH | B. | Ca(OH)2 | C. | NaHCO3 | D. | NaCl |
分析 中和发酵过程产生的酸,又能引起发泡作用,说明该物质与酸反应时生成了气体.
解答 解:A、氢氧化钠具有极强的腐蚀性,不能用于食品工业,故A错误;
B、氢氧化钙具有腐蚀性,不能用于食品工业,故B错误;
C、碳酸氢钠可以与酸反应生成二氧化碳气体,符合题意,故C正确;
D、氯化钠与酸不反应,故D错误,
故选C.
点评 本题考查了常见物质的用途,完成此题,可以依据物质的性质进行.

练习册系列答案
相关题目
1.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 mol NO中含有的原子数目为2NA | |
| B. | 常温下,22.4L氮气含有的原子数目为2NA | |
| C. | 1L1 mol L-1 MgS04溶液中含有的Mg2+数目为2NA | |
| D. | 2.8 g硅单质与足量氧气在高温下完全反应时,硅原子失去的电子数目为2NA |
18.下列过程中反应离子方程式正确的是( )
| A. | 用漂白液漂洗衣物:H2O+2NaClO+CO2═2HClO+CO32-+2Na+ | |
| B. | 用碳酸钠溶液浸泡锅炉水垢:CaSO4(S)+CO32-(aq)?CaCO3(S)+SO42-(aq) | |
| C. | 用氢氧化钠溶液处理工业含二氧化硫的尾气:SO2+2OH-═HSO3-+H2O | |
| D. | 用加少量铁粉的方法存放硫酸亚铁溶液:Fe3++Fe═2Fe2+ |
5.在一定条件下,氯气与碘单质反应,可得到红棕色液体ICl.ICl可发生如下反应:
①2ICl+2Zn═ZnCl2+ZnI2;
②ICl+H2O═HCl+HIO
下列叙述不正确的是( )
①2ICl+2Zn═ZnCl2+ZnI2;
②ICl+H2O═HCl+HIO
下列叙述不正确的是( )
| A. | ICl中含有极性共价键 | |
| B. | 反应①中,当转移0.4mol电子时生成13.6g ZnCl2 | |
| C. | 反应②中,ICl既是氧化剂又是还原剂 | |
| D. | ICl与NaOH反应的化学方程式是:ICl+2NaOH═NaCl+NaIO+H2O |
15.下列说法正确的是( )
| A. | Fe3+具有氧化性,可用KSCN溶液鉴别Fe3+ | |
| B. | H+、Na+、Fe2+、MnO4-在水溶液中不能大量共存 | |
| C. | 磁性氧化铁溶于稀硝酸的离子方程式:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| D. | 将水蒸气通过灼热的铁粉,粉末变红,说明铁与水蒸气在高温下发生反应 |
2.二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中能对二者进行鉴别的是( )
①质谱法
②红外光谱法
③核磁共振氢谱
④李比希燃烧法
⑤元素分析仪.
①质谱法
②红外光谱法
③核磁共振氢谱
④李比希燃烧法
⑤元素分析仪.
| A. | ①② | B. | ④⑤ | C. | ②③ | D. | ③④ |
19.下列有关实验的说法正确的是( )
| A. | 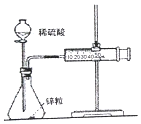 图中测定锌粒与1 mol•L-1 稀硫酸的反应速率,只需测定注射器中收集氢气的体积 | |
| B. | 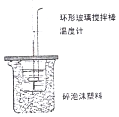 图 装置中进行50 mL 0.50 mol•L-1盐酸与50 mL 0.55 mol•L-1 NaOH 溶液发生中和反应放出热量的测定,使温度计温度升高的热量就是中和反应生成1 mol 水的热量 | |
| C. | 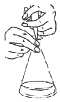 图 酸碱中和滴定中,可以在滴定过程中用少量水冲洗锥形瓶内壁 | |
| D. | 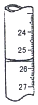 图滴定管中液面位置如图所示,则此时的读数为26.50 mL |
14.常温下,浓度均为0.1mol•L-1 的下列三种盐溶液,其pH 测定如表所示:
下列说法正确的是( )
| 序号 | ① | ② | ③ |
| 溶液 | CH3COONa | Na2CO3 | NaClO |
| pH | 8.8 | 11.6 | 10.3 |
| A. | 三种溶液中,水的电离程度①>③>② | |
| B. | Na2CO3 和NaHCO3 溶液中,粒子种类相同 | |
| C. | Na2CO3 溶液中,c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | 常温下,等浓度的CH3COOH 溶液和HClO 溶液的酸性:HClO>CH3COOH |
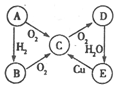 A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.