题目内容
乙烷和丙烷的混合气体完全燃烧后,先将产物通过浓H2SO4,浓H2SO4增重A.1∶1 B.2∶
解析:浓H2SO4增重
2CO2+2Na2O2![]() 2Na2CO3+O2 Δm(固)
2Na2CO3+O2 Δm(固)
2×44 56
m(CO2) 2.24
所以m(CO2)=
设:C2H6x mol, C3H8y mol,则
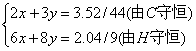
所以x=1/50 mol,y=1/75 mol
所以x∶y=3∶2
答案:C

练习册系列答案
相关题目
题目内容
乙烷和丙烷的混合气体完全燃烧后,先将产物通过浓H2SO4,浓H2SO4增重A.1∶1 B.2∶
解析:浓H2SO4增重
2CO2+2Na2O2![]() 2Na2CO3+O2 Δm(固)
2Na2CO3+O2 Δm(固)
2×44 56
m(CO2) 2.24
所以m(CO2)=
设:C2H6x mol, C3H8y mol,则
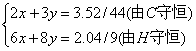
所以x=1/50 mol,y=1/75 mol
所以x∶y=3∶2
答案:C
