题目内容
6.Na2FeO4可通过电解法制备,装置如图,下列说法正确的是( )
| A. | Pt周围的pH降低 | |
| B. | 当生成标准状况下22.4LH2时,转移的电子数为1.5 NA | |
| C. | 阳极反应式是Fe-6e-+8OH-═FeO42-+4H2O | |
| D. | 制得1mol Na2FeO4,有8molOH-从左向右通过离子交换膜 |
分析 整个装置用于制备高铁酸钠,根据装置图,其中阳极为Fe极,是活泼金属作为电极,注意介质是强碱性,因此电解时阳极发生反应:Fe-6e-+8OH-=FeO42-+4H2O,阴极发生反应:2H2O+2e-=2OH-+H2↑,据此分析.
解答 解:A.Pt电极为阴极,阴极是物质得到电子被还原,发生还原反应,考虑到溶液是碱性,因此阴极发生的电极反应为:2H2O+2e-=2OH-+H2↑,反应产生了OH-,因此Pt周围的pH升高,故A错误;
B.当生成标况下22.4LH2时,即H2的物质的量为$\frac{22.4L}{22.4L/mol}=1mol$,阴极发生的电极反应为:2H2O+2e-=2OH-+H2↑,因此反应转移的电子数为2mol,即2NA,故B错误;
C.阳极是Fe作为电极,是活性电极,在NaOH浓溶液中,电解生成Na2FeO4,因此阳极的电极反应式为:Fe-6e-+8OH-═FeO42-+4H2O,故C正确;
D.阳极反应式为:Fe-6e-+8OH-═FeO42-+4H2O,当值得1molNa2FeO4时,同时阳极生成8molOH-,根据电子守恒,此时阴极生成6molOH-,并没有8molOH-从左向右通过离子交换膜,故D错误.
故选C.
点评 本题考查电解原理,牢牢把握住电子守恒,分析电解时的离子运动规律,注意溶液是强碱性的,是OH-参与反应或生成OH-.题目难度不大,是基础题.

练习册系列答案
相关题目
5.关于化学键的各种叙述中正确的是( )
| A. | 离子化合物里一定不存在共价键 | |
| B. | 共价化合物里一定不存在离子键 | |
| C. | 非极性键只存在于双原子的单质分子里 | |
| D. | 由不同元素组成的多原子分子里,一定只存在极性键 |
6.下面是用硫酸钙生产硫酸、漂白粉等一系列物质的流程图.下列说法正确的是( )

| A. | CO、SO2、SO3均是酸性氧化物 | |
| B. | 图示转化反应均为氧化还原反应 | |
| C. | 工业上用氯气和石灰乳制取漂白粉的反应中原子利用率为100% | |
| D. | 严禁用工业酒精勾兑饮用酒是因为工业酒精中含有有毒的甲醇 |
3.X、Y、Z、W、Q都是短周期主族元素,其中X是短周期原子半径最大的元素,X与Y处于同一周期,Y与Z同主族且能形成两种常见的化合物,W能形成两种简单的离子,Q原子的电子总数等于其电子层数的3倍.则下列说法正确的是( )
| A. | 元素Q是短周期非金属性最强的元素 | |
| B. | Y、Z形成的化合物中只有一种属于酸性氧化物 | |
| C. | Y、Z、Q分别与W形成的化合物中,Z形成的化合物的沸点最低 | |
| D. | X分别与Y、Z、W形成的化合物中可能既含离子键又含共价键 |
1.下列各组离子一定能大量共存的是( )
| A. | 在强碱溶液中:Na+.K+.AlO2-.CO32- | |
| B. | 在含大量Fe3+的溶液中:NH4+.Na+.Cl-.SCN- | |
| C. | 在c(H+)=10-13mol/L 的溶液中:NH4+.Al3+.SO42-.NO3- | |
| D. | 在pH=1的溶液中:K+.Fe2+.Cl-.NO3- |
18. (1)科学家寻找高效催化剂,通过如下反应实现大气污染物转化:
(1)科学家寻找高效催化剂,通过如下反应实现大气污染物转化:
2CO(g)+2NO(g)?N2(g)+2CO2(g)△H1
已知:CO燃烧热△H2=-283kj/mol
N2(g)+O2(g)=2NO(g)△H3
几种化学键的键能数据如表一:
表一:
上述△H3=+183kJ•moL-1,△H1=-749kJ•moL-1.
(2)NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划.在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行下述反应I,测得不同时间的NH3和O2的浓度如表:
表二:
则下列有关叙述中正确的是AD
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4υ正(NH3)=6υ逆(H2O)时,说明反应已达平衡
C.当容器内$\frac{n(NO)}{n(N{H}_{3})}$=1时,说明反应已达平衡
D.前10分钟内的平均速率υ(NO)=0.088mol•L-1•min-1
(3)氨催化氧化时会发生下述两个竞争反应I、II.催化剂常具有较强的选择性,即专一性.已知:反应I:4NH3(g)+5O2(g)$?_{高温}^{Pt/Ru}$ 4NO(g)+6H2O(g)
反应II:4NH3(g)+3O2(g)$?_{高温}^{Cu/TiO_{2}}$ 2N2(g)+6H2O(g)
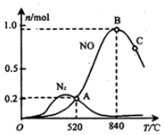
为分析某催化剂对该反应的选择性,在1L密闭容器中充入1mol NH3和2mol O2,测得有关物质的量关系如图:
①该催化剂在高温时选择反应I(填“I”或“II”).
②520℃时,4NH3+3O2?2N2+6H2O的平衡常数K=$\frac{0.{2}^{4}×0.{9}^{6}}{0.{4}^{4}×1.4{5}^{5}}$(不要求得出计算结果,只需列出数字计算式).
③由图象可判断,反应I正反应△H<0(填“>”、“<”或“=”)
④C点比B点所产生的NO的物质的量少的主要原因升高温度平衡逆向移动.
(4)羟胺(NH2OH)的电子式 ,羟胺是一种还原剂,现用25.00mL 0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.50mL0.020mol/L的KMnO4酸性溶液完全作用,则在上述反应中,羟胺的氧化产物是N2O.
,羟胺是一种还原剂,现用25.00mL 0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.50mL0.020mol/L的KMnO4酸性溶液完全作用,则在上述反应中,羟胺的氧化产物是N2O.
 (1)科学家寻找高效催化剂,通过如下反应实现大气污染物转化:
(1)科学家寻找高效催化剂,通过如下反应实现大气污染物转化:2CO(g)+2NO(g)?N2(g)+2CO2(g)△H1
已知:CO燃烧热△H2=-283kj/mol
N2(g)+O2(g)=2NO(g)△H3
几种化学键的键能数据如表一:
表一:
| 化学键 | N≡N | O=O | NO中氮氧键 |
| 键能(kJ/mol) | 945 | 498 | 630 |
(2)NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划.在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行下述反应I,测得不同时间的NH3和O2的浓度如表:
表二:
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| c(NH3)/mol•L-1 | 1.00 | 0.36 | 0.12 | 0.08 | 0.0072 | 0.0072 |
| c(O2)/mol•L-1 | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4υ正(NH3)=6υ逆(H2O)时,说明反应已达平衡
C.当容器内$\frac{n(NO)}{n(N{H}_{3})}$=1时,说明反应已达平衡
D.前10分钟内的平均速率υ(NO)=0.088mol•L-1•min-1
(3)氨催化氧化时会发生下述两个竞争反应I、II.催化剂常具有较强的选择性,即专一性.已知:反应I:4NH3(g)+5O2(g)$?_{高温}^{Pt/Ru}$ 4NO(g)+6H2O(g)
反应II:4NH3(g)+3O2(g)$?_{高温}^{Cu/TiO_{2}}$ 2N2(g)+6H2O(g)
为分析某催化剂对该反应的选择性,在1L密闭容器中充入1mol NH3和2mol O2,测得有关物质的量关系如图:
①该催化剂在高温时选择反应I(填“I”或“II”).
②520℃时,4NH3+3O2?2N2+6H2O的平衡常数K=$\frac{0.{2}^{4}×0.{9}^{6}}{0.{4}^{4}×1.4{5}^{5}}$(不要求得出计算结果,只需列出数字计算式).
③由图象可判断,反应I正反应△H<0(填“>”、“<”或“=”)
④C点比B点所产生的NO的物质的量少的主要原因升高温度平衡逆向移动.
(4)羟胺(NH2OH)的电子式
 ,羟胺是一种还原剂,现用25.00mL 0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.50mL0.020mol/L的KMnO4酸性溶液完全作用,则在上述反应中,羟胺的氧化产物是N2O.
,羟胺是一种还原剂,现用25.00mL 0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.50mL0.020mol/L的KMnO4酸性溶液完全作用,则在上述反应中,羟胺的氧化产物是N2O.
16.五种短周期主族元素A、B、C、D、E的原子序数依次增大,A2属于绿色燃料,C的氧化物用于生产光导纤维,D元素原子的核电荷数是同主族上一周期元素的2倍,B、C为同周期元素,B、D原子最外层电子数之和等于E的最外层电子数. 根据以上叙述,下列说法中正确的是( )
| A. | 五种元素中有两种金属元素 | |
| B. | 元素C、D、E的最高价氧化物对应水化物的酸性增强 | |
| C. | 元素D、E分别与元素A形成化合物的稳定性:A2D>AE | |
| D. | 元素B、D、E的简单离子半径大小为:B>D>E |