题目内容
 为研究水滑石的组成、结构和性质,某校研究性学习小组取得了二种牌号的水滑石样品拟进行探究,请你参与探究并回答相关问题.
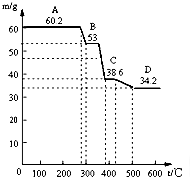
为研究水滑石的组成、结构和性质,某校研究性学习小组取得了二种牌号的水滑石样品拟进行探究,请你参与探究并回答相关问题.(1)甲同学取天然水滑石样品进行恒重分析,已知天然水滑石的化学式可表示为:6MgO?Al2O3?CO2?12H2O,取0.1mol水滑石进行加热时,温度与剩余固体质量的关系如图,平行线上的数字表示残留固体的质量.
当温度在0~280℃质量不变,是什么原因:
A→B减少的物质及其物质的量为:
C→D减少的物质及其物质的量为:
D处化学组成为:
(2)乙组取的CA(美国化学文摘)登记号为12304-65-3的合成水滑石样品,现只知其化学式为:MgaAlb(OH)C(CO3)d,a+b+c+d=25,a、b、c、d为正整数.取该水滑石样品0.1mol,用1mol/L盐酸使其完全溶解.
①消耗盐酸的体积至少为:
②若参加反应的盐酸的物质的量与生成CO2的物质的量之比为18:1,则该水滑石的化学式为:
考点:探究物质的组成或测量物质的含量,镁、铝的重要化合物
专题:实验探究和数据处理题
分析:(1)首先要知道水滑石加热到一定温度才能发生分解,包括1、热分解脱水,2、脱CO32-.在空气中低于280οC时,无影响,当加热到B时,失去部分结晶水;加热到D时,失去CO2,生成金属复合物在加热过程中,可通过差量法求得化学式.
(2)据方程式:MgaAlb(OH)c(CO3)d+(2a+3b)HCl=bAlCl3+aMgCl2+(a+
b+
c)H2O+dCO2↑,计算耗酸量,
1 (2a+3b) d
根据参加反应的盐酸的物质的量与生成CO2的物质的量之比为18:1及化合价代数和为0和已知关系列方程组
则有:
=
,2a+3b=c+2d,a+b+c+d=25
故解得:a:b:c:d=6:2:16:1,故水滑石的化学式为:Mg6Al2(OH)16CO3.
(2)据方程式:MgaAlb(OH)c(CO3)d+(2a+3b)HCl=bAlCl3+aMgCl2+(a+
| 3 |
| 2 |
| 1 |
| 2 |
1 (2a+3b) d
根据参加反应的盐酸的物质的量与生成CO2的物质的量之比为18:1及化合价代数和为0和已知关系列方程组
则有:
| 2a+3b |
| d |
| 18 |
| 1 |
故解得:a:b:c:d=6:2:16:1,故水滑石的化学式为:Mg6Al2(OH)16CO3.
解答:
解:(1)水滑石加热到一定温度才能发生分解,如图所示: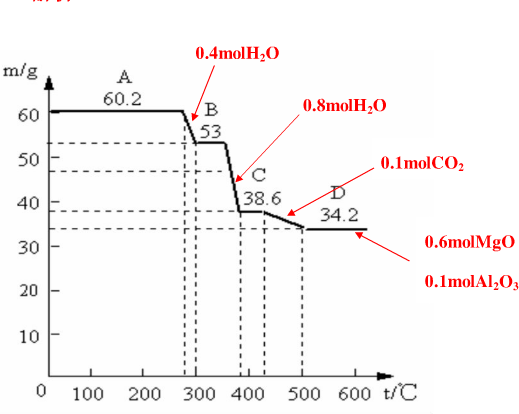
天然水滑石在加热时,A→B发生分解,失去结晶水,n(H2O)=
=0.4mol,C→D发生分解生成CO2,n(CO2)=
=0.1mol;失去结晶水和CO2后,故D处化学组成为:6MgO?Al2O3,
故答案为:天然水滑石在温度低于280℃是稳定的;0.4molH2O;0.1molCO2;6MgO?Al2O3;
(2)据方程式:MgaAlb(OH)c(CO3)d+(2a+3b)HCl=bAlCl3+aMgCl2+(a+
b+
c)H2O+dCO2↑,
1 (2a+3b) d
1mol水滑石消耗(2a+3b)mol盐酸,则0.1mol水滑石消耗(0.2a+0.3b)mol盐酸,消耗盐酸体积为:
=(0.2a+0.3b)L,
则有:
=
据化合价代数和为0,则有:2a+3b=c+2d
又有:a+b+c+d=25
故解得:a:b:c:d=6:2:16:1,故水滑石的化学式为:Mg6Al2(OH)16CO3,
故答案为:0.2a+0.3b;Mg6Al2(OH)16CO3.

天然水滑石在加热时,A→B发生分解,失去结晶水,n(H2O)=
| (60.2-53)g |
| 18g/mol |
| 38.6g-34.2g |
| 44g/mol |
故答案为:天然水滑石在温度低于280℃是稳定的;0.4molH2O;0.1molCO2;6MgO?Al2O3;
(2)据方程式:MgaAlb(OH)c(CO3)d+(2a+3b)HCl=bAlCl3+aMgCl2+(a+
| 3 |
| 2 |
| 1 |
| 2 |
1 (2a+3b) d
1mol水滑石消耗(2a+3b)mol盐酸,则0.1mol水滑石消耗(0.2a+0.3b)mol盐酸,消耗盐酸体积为:
| (0.2a+0.3b)mol |
| 1mol/L |
则有:
| 2a+3b |
| d |
| 18 |
| 1 |
据化合价代数和为0,则有:2a+3b=c+2d
又有:a+b+c+d=25
故解得:a:b:c:d=6:2:16:1,故水滑石的化学式为:Mg6Al2(OH)16CO3,
故答案为:0.2a+0.3b;Mg6Al2(OH)16CO3.
点评:本题考查了复杂化学式的计算,看图分析等知识,题目难度稍大,试题涉及的计算量较大,解题过程中需要有较强的耐心,试题培养了学生的分析、理解及化学计算能力.分析图象信息是完成本题目的关键.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
烧碱、醋酸和碳酸氢钠等是生活中的常见物质.下列有关它们的表述正确的是( )
| A、将醋酸逐滴加入醋酸钠溶液中至溶液呈酸性,则该混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B、将0.1 mol?L-1 CH3COOH溶液加水稀释,在此过程中,醋酸的电离程度、溶液的pH都逐渐增大 |
| C、在碳酸氢钠溶液中加入与其等物质的量的烧碱,溶液中的阴离子只有CO32-和OH- |
| D、常温下,将pH=12的烧碱溶液与pH=2的醋酸溶液等体积混合,所得混合液的pH>7 |
巴豆酸的结构简式为CH3-CH=CH-COOH,现有①氯化氢 ②溴水 ③纯碱溶液 ④2-丙醇 ⑤酸化的高锰酸钾溶液.试根据其结构特点判断在一定条件下能与巴豆酸反应的物质组合是( )
| A、②④⑤ | B、①③④ |
| C、①②③④ | D、①②③④⑤ |


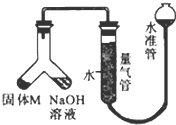 某课外兴趣小组为探究某种铝合金(合金元素为Mg 和Al)是否符合国家质量标准(国家规定其中铝含量不能低于78%),设计如图装置进行实验.
某课外兴趣小组为探究某种铝合金(合金元素为Mg 和Al)是否符合国家质量标准(国家规定其中铝含量不能低于78%),设计如图装置进行实验.