题目内容
碳化钙(电石)是一种离子化合物.下列说法正确的是( )
| A、C22-与CN-两种微粒具有相同的电子数 | B、C22-的电子式是: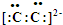 | C、碳化钙与水的反应属于氧化还原反应 | D、晶体中的CaC2是一种极性分子 |
分析:A.C22-与CN-两种微粒核外电子数都是14;
B.该离子两个碳原子之间存在共价三键;
C.CaC2+2H2O=Ca(OH)2+C2H2↑;
D.CaC2是离子晶体.
B.该离子两个碳原子之间存在共价三键;
C.CaC2+2H2O=Ca(OH)2+C2H2↑;
D.CaC2是离子晶体.
解答:解:A.C22-与CN-两种微粒为等电子体,核外电子数都是14,故A正确;
B.该离子两个碳原子之间存在共价三键,电子式为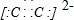 ,故B错误;
,故B错误;
C.CaC2+2H2O=Ca(OH)2+C2H2↑,该反应中没有电子转移,不属于氧化还原反应,故C错误;
D.CaC2是由阴阳离子构成的,属于离子晶体,故D错误;
故选A.
B.该离子两个碳原子之间存在共价三键,电子式为
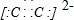 ,故B错误;
,故B错误;C.CaC2+2H2O=Ca(OH)2+C2H2↑,该反应中没有电子转移,不属于氧化还原反应,故C错误;
D.CaC2是由阴阳离子构成的,属于离子晶体,故D错误;
故选A.
点评:本题以碳化钙为载体考查了晶体类型的判断、氧化还原反应、电子式的书写等知识点,根据这几个概念的内涵来分析解答,易错选项是B,会书写其电子式,为易错点.

练习册系列答案
相关题目
